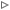Внимание! Теперь для входа на форум необходимо вводить единый пароль регистрации сервисов sibnet.ru! Здравствуйте, гость ( Вход | Регистрация )
| |||||||||||||||||||||||||||||||||||||||||||
  |
| akvamistika |
 15.11.2008, 14:00 15.11.2008, 14:00
Сообщение
#1
|
 Аквариумисты Сибири - объеденяйтесь !!!    Группа: VIP Сообщений: 8 900 Регистрация: 28.8.2007 Из: СССР Пользователь №: 4 944 |
Мы часто мало обращаем внимание на состав воды и поэтому у нас возникают всевозможные проблемы с содержанием аквариуных обитателей и расстений.
У кого есть литература по данному вопросу - делимся, кто может поделиться опытом - советуем. АКВАРИУМНАЯ ГИДРОХИМИЯ Состав аквариумной воды: основные проблемы Краткая "шпаргалка" на наиболее типовые случаи плохого самочувствия рыб » Спойлер (нажмите, чтобы прочесть) « Вопрос на нашем форуме: "Как начинающий сталкиваюсь с такой проблемой :-) сейчас к счастью недостатка в литературе нет, на мой взгляд, взгляд новичка и дилетанта в вопросах касаемых содержания аквариума, её даже с избытком, но я нигде не видел чего-нибудь наподобие систематической таблицы, в которой были бы расписаны основные аквариумные проблемы и способы их устранения, связанные с составом воды. Например: нитраты - влияют на то и на то... Допустимая концентрация столько-то, превышение влияет на то-то и то-то, проявляется так-то и так-то... - измерить так и так... Увеличить концентрацию таким-то способом. Уменьшить - таким-то. Было бы огромным подспорьем для начинающих иметь такую таблицу под рукой. С уважением, Александр". Идея хороша, но реализовать ее не так-то легко. Можно разве что сделать "шпаргалку" на наиболее типовые случаи. Отчасти это уже реализовано в статье "5 параметров...". И все же, более сложных, не типовых случаев куда больше. Всегда есть нюансы в каждой отдельной ситуации. Биология вроде бы наука точная, но уж очень много факторов действует одновременно. Аквариумистика ближе к биологии, чем к какой-либо науке еще. К химии тоже близка, но гидрохимия "подарочек" тот еще – не слаще биологии. Поэтому контролировать развитие вашего аквариума в нужном вам направлении нелегко. Для этого необходимо понимать суть того, что происходит в аквариуме, что именно можно измерить, какие выводы из полученных данных можно сделать и какие действия затем предпринять. Именно поэтому я и взялся писать цикл статей по гидрохимии. Надеюсь, что хоть кому-то они окажутся полезными. А пока все-таки приведу здесь "шпаргалку": 1. ОЧЕНЬ КИСЛАЯ ВОДА. Рыба "зажата", стоит на месте, совершает однообразные движения, либо движется рывками. Может быть покрыта слизью. Жабры темные. Дыхание часто очень замедленное. Точно убедиться, что вода скисла можно только с помощью теста на рН. Обнаружив в своем аквариуме эту неприятность надо осторожно начать подмену воды. За день нельзя поднимать рН больше чем на 1.5 единицы. Ни в коем случае нельзя переводить рыб сразу из кислой воды в щелочную. Если бороться с закислением с помощью соды (питьевая сода - 0.5 чайной ложки на 20-40 л), то надо сильно аэрировать аквариум. Любители фирменной аквариумной химии могут для определения рН воспользоваться тестом от Aquarium Pharmaceuticals, однако, НАШ рН-тест работает в более широком диапазоне и раз в 5 дешевле. 2. ОЧЕНЬ ВЫСОКАЯ ОКИСЛЯЕМОСТЬ ВОДЫ. Что это такое описано в уже упоминавшейся статье "5 параметров...". Часто это несчастье развивается вместе с закисанием воды. Меры борьбы: внесение в аквариум марганцовки до слабого розового цвета и дальнейшая замена воды. Можно воспользоваться фирменным средством ВIO-СНЕМ ZORB. Когда нормальные параметры рН и окисляемости будут достигнуты, необходимо воспользоваться средствами типа нитривек или STRESS ZYME, либо активным илом из фильтра благополучного аквариума. Регулярная подмена воды (15-25% еженедельно), чистка грунта и умеренное кормление высококачественными кормами (от хороших фирм, либо НАШИМ), не "растворяющимися" в воде и не дающими обилия мелких частиц, которые забиваются в фильтр и грунт. 3. ВЫСОКИЙ УРОВЕНЬ АММИАКА. Концентрация более 0.5 мг/л аммония опасна. Содержание непосредственно аммиака зависит от рН и концентрации аммония, но, в первом приближении, не надо превышать указанный порог по аммонию. Определить концентрацию аммиака/аммония можно с помощью FRESHWATER AMMONIA TEST KIT. С помощью несравненно более дешевого реактива НЕССЛЕРА, можно надежно тестировать опасные уровни аммиака и аммония. Жабры рыб при отравлении аммиаком - лиловые. При отравлении аммиаком необходима немедленная замена воды. Часто бывает эффективно использовать марганцовку в интервалах между заменами. Сначала придется сделать несколько замен в день. Для предотвращения повторных аммиачных ударов в фильтры надо положить цеолитный наполнитель. Использовать нитривек или STRESS ZYME, активный ил. Фильтрация воды через цеолит может быстро снизить концентрацию аммиака. Кроме того, для этой цели можно воспользоваться средством AMMO-LOCK 2, а быстро улучшить самочувствие рыбок после аммиачного отравления поможет STRESS COAT. Последнее средство нейтрализует и аммиак тоже. Это вообще хороший препарат, помогающий от всех бед. Небольшое подсаливание воды (1 чайная ложка поваренной соли на 20 л) улучшает самочувствие рыб. Если в аквариуме есть сомики-коридорасы, то солить НЕЛЬЗЯ! 4. ВЫСОКИЙ УРОВЕНЬ НИТРИТОВ. Уже опасно, если больше 0.1 мг/л. Обычно выше 0.2 мг/л не надо бы. Все уже очень плохо, если более 1 мг/л. Рыбки темнеют, стоят носами в углы аквариума. Жабры коричневатые. Не едят или едят плохо. Чуть что - начинают задыхаться. Далее идут вспышки бактериальных инфекций. Определить, что по нитритам перебор можно с помощью специальных тестов (FRESH & SALTWATER NITRITE TEST KIT). При обнаружении опасного уровня нитритов надо начать осторожно подменивать воду. Заодно ее надо подсолить (до 0.5-1 г в литре), если вода мягкая, то поднять жесткость до 2-3 мг-экв/л. Использовать для поднятия жесткости хлористый кальций. Не поднимать больше, чем на 1 мг-экв/л за 6-10 часов. Очень полезно использовать марганцовку в интервалах между сменами воды. Главная ошибка новичков, приводящая к гибели рыбы - быстрая замена воды. Нельзя за раз менять больше одной четверти объема. Даже после выхода на нормальную гидрохимию, после этого катаклизма рыба может длительное время болеть. Часто разрушаются жаберные лепестки. Развиваются сложные бактериальные инфекции. Лучшее средство лечения - цифран с метронидазолом из обычной аптеки. Дозировки от 1 г в 100 л цифрана и 50 мг метронидазола на 100 л. При восстановительной терапии хорош ALL-NATURAL MELAFIX. 5. ВЫСОКИЙ УРОВЕНЬ НИТРАТОВ. Новая рыба не "идет" в такой аквариум. Старожилы живут, но все хуже едят. Особо критично для дискусов и прочих обитателей бассейна Амазонки. При обнаружении с помощью теста (например, FRESH & SALTWATER NITRATE TEST KIT), надо начать менять воду. Можно менять сразу много (если конечно уверены в качестве новой воды, если в ней будет много аммиака и аммония, что не редкость, то массовое унитазирование сдохших рыб будет неизбежно…). После мытья фильтров и подмены воды рН может заметно возрасти. В итоге, аммиак и нитраты будут действовать на рыб одновременно. Это классическое "попадалово" наших доблестных аквадизайнеров, которые норовят приходить к клиенту раз в две недели и менять сразу треть объема водой, только пропущенной через угольный фильтр и немного согретой. Аммиак при этом в воде как был так и остается, а нитраты в аквариуме за две недели успевают накопиться, особенно если сердобольные хозяева кормят любимцев как на убой. Подмена воды приводит к тому, что спустя час-два рыбки начинают вяло плавать у поверхности воды. А происходит вот что: подмена воды снизила концентрацию нитратов всего лишь на одну треть, но концентрация аммиака поднялась в несколько раз. Он попал в аквариум вместе со свежей водой и его выделили рыбы. Мытые биофильтры заметно теряют эффективность, не окисляют аммиак с нужной скоростью. Вот тут обычно рыбок и солят - это обычное народное средство: если рыбкам плохо, то воду надо подсолить. СОЛИТЬ ВОДУ ПРИ НИТРАТНОМ ОТРАВЛЕНИИ НЕЛЬЗЯ!!!! Ну а далее - печальное унитазирование.* И ведь что обидно: все жило, но вот пришли "специалисты" поменяли воду и все сдохло… Продвинутые дизайнеры успешно избегают неприятностей используя средство STRESS COAT от A.P. Однако, нитраты при этом, как были в воде аквариума, так и есть. Рыбы остаются ослабленными, а вьетнамка процветает. Опасный уровень нитратов – более 50 мг в литре, но для разных видов он очень различается. Говорят, что карпы держат и 800 мг в литре. В аквариумах с золотыми рыбками 200 мг в литре не редкость. Они от этого сразу не мрут, но им это вредно. Вскоре появляются "перевертыши" - те, что после еды начинают плавать животом кверху. 6. ОЧЕНЬ ВЫСОКИЙ УРОВЕНЬ РН. Рыба бледная и растопыренная. Нарушается координация движений. Забивается в заросли и там умирает. Наверняка диагноз можно поставить только при выполнении теста на рН. Можно воспользоваться более точно работающим в области высоких значений рН фирменным специальным тестом FRESH & SALTWATER HIGH RANGE pH TEST KIT. Обычно неприятности начинаются при значениях рН выше 8-8.5. Но все зависит от вида рыбы. Можно довольно быстро путем смены воды опустить рН к 8. При этом значении рН могут выжить почти все. Полезно добавление в воду витаминов группы В. Есть средства "ФИШТАМИН" и STRESS COAT, позволяющие быстро провести восстановительную терапию. В дальнейшем подмены стоит делать кипяченой водой. Если есть искус снизить рН путем добавления кислоты, то должна быть обеспечена сильная аэрация аквариума. Кислоту (лучше соляную) надо добавлять очень осторожно. Известняковый грунт и камни из аквариума убрать. Есть фирменное средство "рН минус". Фирма Aquarium Pharmaceuticals (A.P.) выпускает специальные буферные растворы, позволяющие стабилизировать значения рН на оптимальном для конкретных групп рыб уровне, и подлечить бедных рыбок от последствий воздействия воды с высоким уровнем рН. Узнать об этих препаратах и получить их по почте можно здесь. 7. ОТРАВЛЕНИЯ ТЯЖЕЛЫМИ МЕТАЛЛАМИ. Улитки ампуллярии с трудом ползают по стеклу, так как их нога плохо прилипает. Дойдя до поверхности остаются там и часто дышат. Усы не расправлены. Видна слизь. Рыба плохо ест, худая. Можно отравить рыбу мотылем и трубочником, пойманными в неблагополучных местах. Симптомы других отравлений очень изменчивы. Меняйте воду, хоть всю сразу, если остальные тесты дают хорошие результаты, а рыбе плохо. Есть кондиционеры для воды, которые обезвреживают тяжелые металлы в воде, например, ТАР WATER CONDITIONER. Можно поднять жесткость воды на 1-1.5 мэкв/л с помощью хлористого кальция. В присутствии ионов кальция в воде тяжелые металлы менее токсичны. 8. СЛИШКОМ МНОГО УГЛЕКИСЛОГО ГАЗА. Более 30 мг/л. Рыба часто и тяжело дышит. Некоторые виды раздуваются и висят у поверхности. Это же происходит с лягушками и тритонами. Встречается редко, если только вы специально воду углекислотой не обогащали. Меры борьбы: прекратить подачу углекислоты, усилить аэрацию, и добавить 3% перекись водорода 20 мл на 100 л. Если вы долго подавали в аквариум углекислый газ, а в аквариуме есть известняк, то после прекращения подачи углекислоты и сильного продувания воды возможен РЕЗКИЙ!!! скачек рН в щелочную сторону. Необходимо контролировать изменения рН, или измерить карбонатную жесткость и воспользоваться таблицей в статье "5 параметров...", чтобы определить до каких величин может скакануть рН. Если этот уровень окажется слишком большим, то надо будет в нужный момент воспользоваться буферными растворами, средством рН-, отваром торфа, ольховыми шишечками, мхом сфагнумом и другими средствами. Вот такая шпаргалка. Надеюсь, что со временем об этом всем расскажу подробно. В. Ковалёв, кандидат биологических наук. * Дополнение, написанное 4 месяца спустя, после опубликования этого материала. В этом материале я не ставил целью доказательно объяснить все эффекты интоксикации рыб, здесь упомянутые. Шпаргалка есть шпаргалка и не более того. Это всего лишь руководство по экстренным действиям для новичков. Отрадно, что многим это руководство на САМОМ ДЕЛЕ ПОМОГЛО! И это понятно, ведь написано оно на ПРИМЕРЕ РЕАЛЬНЫХ случаев из практики аквариумистов. Однако, недавно мне показали обсуждение этой статьи на одном известном форуме. Мне казалось, что написал я тут все предельно понятно, ан нет! Оказалось, что не очень. Вот для особо непонятливых объясню еще раз раздел про отравление НИТРАТАМИ. Откуда берется аммиак и чем все же травятся рыбы? Хроническое отравление нитратами снижает способность рыб противостоять всем прочим невзгодам. А концентрация аммиака возрастает из-за: 1. - повышения рН воды (аммоний переходит в более токсичный аммиак); 2. - временного снижения эффективности работы нитрифицирующих бактерий в грунте и фильтре (их сифонили и мыли); 3. - разложения хлораминов из только что залитой водопроводной воды (об этом можно прочитать еще и здесь). Для отравленных нитратами рыб даже очень незначительного возрастания концентрации аммиака достаточно, чтобы они почувствовали себя плохо. Далее, если аквариум с высокой концентрацией нитратов посолить - рыбы могут сдохнуть. Подтверждение своих наблюдений я нашел в книге Спотта "Содержание рыбы в замкнутых системах", "Лесная и пищевая промышленность", 1983 год, страница 132. Где приведены экспериментальные научные данные о том, что в солоноватой воде токсичность нитратов возрастает. Ваш В.К. (31.10.03) АКВАРИУМНАЯ ГИДРОХИМИЯ Кислотный дождь. Что может содержать дождевая и талая вода, как проверить пригодна ли она для нереста аквариумных рыб и почему весной качество водопроводной воды может резко ухудшиться. » Спойлер (нажмите, чтобы прочесть) « Если вы живете в регионе с жесткой сильно минерализованной водой, то использование в аквариуме дождевой воды, может быть, будет и не плохим вариантом. Смесь дождевой и водопроводной воды вполне пригодна для жизни большинства аквариумных рыбок. В такой воде вам будет гораздо легче создать условия для нормального роста и развития большинства аквариумных растений. Кроме того, сбор дождевой воды - способ получить мягкую слабокислую воду, пригодную для нереста многих рыб. При этом надо лишь найти подходящую для водосбора чистую поверхность. Не следует собирать воду с крыши, покрытой старым и ржавым листовым железом или новым шифером. Чистая полиэтиленовая пленка вполне подойдет. Конечно же, это "экзотический" по нашим временам способ, но если дистиллированной воды не достать, а установка домашней системы обратного осмоса не по карману, то стоит попробовать. Почему вода получается со слабокислой реакцией? Из-за растворения в капельках дождевой воды углекислого газа (диоксида углерода). Во всех деталях и с расчетами этот процесс описан в одной очень интересной, но немного скучной книге. Здесь я приведу только химическую реакцию, и расскажу о сути дела, а все, интересующиеся точными расчетами, могут сами обратиться к указанной книге, она не библиографическая редкость. Сначала углекислый газ растворяется в воде и некоторая часть его молекул реагирует с водой: CO2+H2O <–> H2CO3 Продукт реакции - угольная кислота, которая в капельке воды диссоциирует на ион водорода и гидрокарбонатный ион: H2CO3 <–> H+ + HCO3- В результате вода становится слегка кислой. Но только слегка, потому что угольная кислота - слабая, и далеко не все её молекулы диссоциируют. Расчеты, сделанные для нормального атмосферного давления и нормального содержания углекислоты в атмосфере, а именно от этого зависит сколько углекислоты растворится, показывают, что значение рН при этом не падает ниже 5.6. Кстати, величины рН=5.7-6.0 характерны и для дистиллированной воды. В ней также растворяется атмосферный углекислый газ. К сожалению, в настоящее время, в атмосфере в качестве закислителя дождевой воды присутствует не только диоксид углерода, но еще и многие другие вещества, например диоксид серы (SO2). В среднем, над индустриальным регионом в воздухе содержится 2.04*10-7 молей SO2. Можно ожидать, что один кубический метр дождевого облака включает в себя около 1 г жидкой воды, т.е. 0,001 дм3. Если бы весь SO2 был перемещен в капельки этой воды и окислен до серной кислоты (H2SO4), то 2,04*10-7 молей серной кислоты растворилось бы в 0,001 дм3 жидкой воды, что дало бы концентрацию в жидкой фазе 2,04*10-4 моль/л. H2SO4 является сильной кислотой, почти все молекулы которой диссоциируют в атмосферных условиях с образованием двух протонов (ионов водорода) и сульфат-иона: H2SO4 –> 2H+ + SO42- Таким образом, концентрация протонов будет 4.08*10-4 моль/л, что соответствует значению рН=3.4. Испарение воды из капелек и дальнейший перенос SO2 из атмосферы в капельки в процессе их падения на землю могут привести к дальнейшему снижению рН. Вывод из всего вышеизложенного таков. Если вы решили использовать дождевую воду, то не собирайте ее сразу после начала дождя, подождите минут 15-20, дождь очищает воздух, так как капли вбирают в себя загрязнители. Все знают как хорошо дышится после дождика! Набрав дождевую воду, обязательно измерьте рН. Вряд ли стоит использовать слишком кислую воду. Данные анализа дождевой воды (по материалам сайта "Аналитическая химия", где приведено много примеров анализа природных пресных вод и еще много других интересных вещей) Дата (1993 г.)Cl, мг-экв/лNO3, мг-экв/лSO4, мг-экв/лNa, мг-экв/лNH4, мг-экв/лМинерализация мг/лpH 9.09-10.090.030.020.020.150.0388.46.51 11.090.0060.0150.0160.140.0346.56.12 12.09-13.090.010.030.020.230.04610.35.97 13.09-14.090.010.010.010.10.024.66.21 21.09-22.090.020.0350.050.140.0816.96.01 Среднее0.0130.0280.0320.150.0449.3-9.56.16 Образцы дождей отбирались за 40 км к югу от г. Новосибирска. Как видно из этих данных, дождевая вода может быть вполне "чистой". Новичкам в аквариумистике содержание этой таблицы будет понятнее, если они прочитают эту статью. Низкие значения рН свидетельствуют о ее сильном загрязнении промышленными выбросами. Даже при смешивании ее с аквариумной водой конечное значение рН может получиться слишком низким и кроме того, в такой воде могут содержаться различные ядовитые вещества. Помните: редкая рыбка выдержит рН ниже 4.5. Если рН дождевой воды окажется в пределах 5.5 - 6.5 эту воду можно использовать для нереста. Для не очень требовательных рыб достаточно просто добавить к аквариумной воде дождевую в пропорции 3:1 или 1:1, чтобы спровоцировать нерест. О том, как приготовить на базе дождевой воды смеси с заданными свойствами или искусственную аквариумную воду рассказано в разделе "Приготовление искусственной аквариумной воды". В дождевой воде может раствориться не только диоксид серы, а много чего еще, поэтому будет невредно проверить ее на окисляемость с помощью описанного здесь теста. Или сразу же профильтровать через активированный уголь. И в заключение, обсудим причины весеннего ухудшения качества воды. Аквариумисты со стажем и особенно разводчики аквариумных рыбок хорошо знают, что это такое. Ситуации бывают просто трагические. Сидит полный аквариум молоди. Чтобы она не "затянулась" ее надо хорошо кормить и менять воду каждый день. Но делать это невозможно - доливание свежей воды тут же приводит к заметному ухудшению самочувствия рыб. Итак, что же происходит весной? После того, как дождевые капли с серной кислотой достигнут земли, может иметь место дальнейшее повышение концентрации кислоты, если вода замерзнет в виде снега. В процессе таяния снега происходит преимущественная потеря растворенных ионов, поскольку они стремятся накапливаться снаружи зерен льда, из которых состоят сугробы. Это означает, что на ранних стадиях таяния выносится именно растворенная серная кислота. Возможно двадцатикратное повышение ее концентрации в талой воде! Это получается уже не просто кислотный дождь, а кислотный потоп. В это время вода в водопроводе может стать гораздо кислее обычного, или содержать повышенное количество аммония и сернокислого алюминия. С помощью сернокислого алюминия воду на водопроводных станциях "коагулируют" - алюминий дает коллоидный осадок, он отфильтровывается сам и заодно извлекает из воды множество других загрязнителей. Но вот если с его дозировкой не угадать, то его остаточные количества попадут в водопроводную сеть. Икра рыб в такой воде оплодотворяется очень плохо, вероятно и рыбам он не нравится. Но главная проблема не в этом. Кислая вода очень плохо коагулируется. Ее приходится специально подщелачивать, как правило это делают с помощью гидроксида аммония (NH4OH) или аммиака. Вот и оказывается он затем в водопроводной воде обычно в виде ионов аммония или хлораминов (они образуются при хлорировании воды, содержащий аммиак и аммоний и постепенно разлагаясь в водопроводе или уже в аквариуме обогащают воду аммиаком). Рыбы в ходе своей жизнедеятельности выделяют в воду все тот же аммоний, воду надо менять, но и в водопроводной воде его не меньше, или только чуть меньше! Есть из этой ситуации выход? В общем-то есть, но об этом - в статье об аммиаке и аммонии. Поделился своими соображениями о причинах весенних проблем у аквариумистов и пересказал главу из книги "Введение в химию окружающей среды" (авторы Дж. Андруз, П. Бримблекумб, Т. Джикелз, П. Лисс, Москва, "Мир", 1999 г.) В. Ковалёв. » Спасибо сказали: «
|
| Necromancer |
 15.11.2008, 20:29 15.11.2008, 20:29
Сообщение
#2
|
 Болтун  Куратор темы Сообщений: 525 Регистрация: 21.3.2008 Из: Новосиб - Барнаул Пользователь №: 26 086 Репутация:  99 99  |
Аквариумная вода
Важнейшие свойства и показатели качества воды в пресноводном аквариуме Введение для аквариумистов-новичков » Спойлер (нажмите, чтобы прочесть) « Как говорят, аквариумная гидрохимия - очень "сухая" тема. Но ведь без неё просто никак нельзя! Я это понял по вопросам, приходящим на наш форум. Жесткость воды, бесчисленное количество всяких разных градусов из разных книжек, разных сайтов, разных стран, как их сопоставить друг с другом и что же они все-таки выражают? Чем жесткость отличается от солености? А если насыпать соли, то рН изменится, или, может быть, стабилизируется? А ведь еще есть такие странные, но вроде бы нужные вещи как редокс потенциал, щелочность и таинственные микросименсы, но не сами по себе, а приходящиеся на 1 см!!! Короче говоря, тема огромная и не веселая, но нужная. Я долго думал с чего бы начать… И начал с самого начала. Надеюсь, что эти материалы окажутся полезными многим аквариумистам-новичкам и профессионалам-эмпирикам. Сразу оговорюсь, в этой статье и во всем данном разделе речь пойдет только о пресной воде, и, следовательно, только о пресноводных аквариумах. Водопроводная вода Для большинства горожан источник пресной воды - это водопроводный кран. Вода к крану подается по трубам, от качества и материала которых, кстати, зависит и качество воды, которая потом окажется в вашем аквариуме. Не меньше, а то больше, зависит от водопроводной станции, где осуществляется обработка воды перед подачей ее в водопроводную сеть. Ну, а на водопроводную станцию, вода попадает чаще всего из какого-либо большого и, по возможности, чистого водоема (реки, озера, водохранилища), или из артезианской скважины. Вода из-под земли может быть минерализована сильнее, чем поверхностные воды в данной местности.  На фотографии вверху изображен носик водопроводного крана с капелькой воды. Капелька прозрачная, на вид - очень даже чистая. Но так только кажется. Прозрачная не значит "чистая". Загляните внутрь носика: толстый рыже-бурый налет на его стенках образован веществами, выделившимися из воды. Пока вода находится в водопроводной системе, одни вещества частично осаждаются на стенках труб, другие, может быть и те же самые, растворяются (направленность процессов определяется главным образом водородным показателем - рН воды и ее окислительно-восстановительным (тем самым "редокс") потенциалом, а они могут изменяться в зависимости от времени года и интенсивности хлорирования, либо озонирования воды. О том, что растворение идет достаточно энергично, свидетельствует "облезлый" носик крана. А ведь это никель растворился - тяжелый металл. Оказавшись в аквариуме, он окажет негативное действие в первую очередь на улиток, а затем и на рыб. Если присмотреться, то можно заметить щербинки и на латунных стенках крана. Под действием воды да еще и соединений хлора (ведь водопроводную воду хлорируют) коррозии подвергается и латунь, а значит в воду переходят медь и цинк. Сами водопроводные трубы могут быть медными или оцинкованными. В старину были еще и свинцовые трубы, например в Московском Кремле. Есть даже мнение, что повышенная нервозность Ивана Грозного связана с потреблением обогащенной свинцом воды. В общем, вода - очень хороший универсальный растворитель, а потому химически чистой воды практически не бывает. Даже в дистиллировке растворен углекислый газ, и не только он один. Ну а в аквариумной воде чего только не "плавает". Поэтому аквариумная гидрохимия - тема обширная. Примеси, содержащиеся в воде, состоят из: 1. Свободных ионов: заряженных положительно катионов и отрицательно - анионов. Растворенные в воде металлы существуют там в виде катионов и комплексных соединений (чаще всего это соединения все тех же катионов с природными органическими кислотами, например, гуминовыми, которыми вода обогащается при фильтрации через почву). Примеси в воде в виде ионов представляют собой истинные растворы. Их невозможно удалить при помощи механической фильтрации. В идеале растворы прозрачны (т.е. мутность отсутствует), но они могут быть окрашенными, так гуминовые кислоты делают воду коричневатой (торфованная вода). Многие органические вещества также растворяются в воде с образованием истинных растворов, например, спирт, глюкоза, различные пестициды, лекарства. Удалить их можно путем фильтрации через активированный уголь. Однако, уголь не удаляет ионы металлов. 2. Взвешенных веществ – это продукты выветривания пород, остатков растений и водных животных, бактерий и других микроорганизмов (фито- и зоопланктон). Наличие этих примесей делает воду мутной, их можно отфильтровать. 3. Коллоидных веществ (солей кремневой кислоты, окиси кремния, гидроокислов железа и алюминия, продуктов разложения микроорганизмов. Наличие этих примесей может быть не заметным для глаза, а может вызывать легкую опалесценцию воды (беловато-матовую мутность, очень характерную для новых аквариумов на 2-ой - 5-й день). 4. Растворенных газов. Для аквариумиста наибольшее значение имеют кислород и углекислый газ. По содержанию этих примесей природные воды заметно отличаются друг от друга. Зачастую эти различия можно выявить только в результате аналитического лабораторного исследования, но иногда они видны и невооруженным глазом.   Слияние левого притока Амазонки "Черной" реки Риу-Негру с Амазонкой (левая фотография) и реки Тапажос (светло-голубые воды) с Амазонкой (фотографии из книги Г.Й.Майланда *). Цвет воды во всех трех реках различен. Выделяют черные, светлые (прозрачные) и белые воды. Первоначально это разделение вод по типам применяли только к бассейну Амазонки, однако в настоящее время оно распространено и на тропические воды других регионов**. "Черных", богатых гуминовыми кислотами болотных вод с кислой реакцией, немало и на севере России, соответственно и Черных речек предостаточно. Для того чтобы сделать этот рассказ более упорядоченным, рискну ввести такие понятия, как природные свойства воды и показатели качества воды. Свойства воды определяются такими ее параметрами, как минерализация, водородный показатель (рН) (рН может выступать и как критерий качества аквариумной воды), постоянная и временная жесткость. Эти параметры отражают природные (естественные) особенности воды для данной местности. Так, например, в реке Неве и в водопроводной сети Санкт-Петербурга вода мягкая и слабо минерализованная, активная реакция (рН) невской и хорошо отстоянной питерской водопроводной воды нейтральная (в случае водопроводной воды это должно получаться в идеале, а на самом деле получается не всегда!). Но в некоторых районах (Петродворцовый, Красносельский) своё автономное водоснабжение и вода там жесткая с рН выше 8. В Москве вода средней жесткости, но тоже местами встречаются "аномалии". В целом, в этом городе она колеблется в интервале 1.8 - 4.6 мг-экв/л (dGH 5-13°). Отсюда вывод: не взирая на "общественное мнение", бытующее в вашей местности относительно основных параметров воды, при первой же возможности постарайтесь определить все сами, или попробуйте получить информацию на местной водопроводной станции. (Если сможете, конечно. Этот, в принципе правильный, совет берет свое начало из западных аквариумных книжек, применительно к российским условиям он выглядит ну просто умилительным, однако, попытка – не пытка.) Теперь поговорим о показателях качества водопроводной воды. И мягкая, и жесткая, как природная, так и водопроводная и аквариумная вода может быть хорошего и плохого качества. Качество в данном случае будет определяться степенью загрязнения воды. Так, например, если в речной воде обнаружены аммоний и нитраты, значит она загрязнена сточными водами (бытовыми, либо сельскохозяйственными, что, собственно, является совершенно обычным делом), качество ее от этого ухудшилось. Если на этой реке установлен водозабор, то эта загрязненная вода будет поступать в водопроводную сеть и в ваш аквариум тоже. Существующие методы водоподготовки не удаляют аммоний и нитраты, напротив, их может стать только больше. Соответственно и качество водопроводной воды будет невысоким. Если вы решили завести дискусов, рыб-слонов, боцию-клоуна, то столкнетесь с большими проблемами - эти рыбы очень не любят азотного загрязнения воды. Качество - понятие относительное, ведь, что для одних организмов хорошо, для других может быть очень даже плохо. С людьми и рыбками по многим показателям качества воды как раз тот самый случай. Для воды, используемой в рыбоводстве, и для водопроводной воды разработаны различные системы нормативов, регламентирующих допустимое содержание различных примесей, то есть установлены ПРЕДЕЛЬНО ДОПУСТИМЫЕ КОНЦЕНТРАЦИИ загрязнителей - ПДК. Так вот, рыбоводные ПДК очень часто в 100, а то и в 1000!!! РАЗ НИЖЕ санитарно-гигиенических водопроводных. Правда, может быть, гигиенистам только так кажется, а на самом деле, люди точно также как и рыбки, травятся свободным хлором и хлораминами, аммиаком, тяжелыми металлами, сернокислым алюминием, органическими флокуллянтами, которые практически всегда есть в водопроводной воде в количествах не превышающих ПДК, установленных для людей. Вот только люди несравненно живучей рыбок и умирают от грязной воды гораздо медленнее. Наверное, у кого-то эта тирада вызовет чувство законного протеста, но все же давайте вспомним, что горцы (и отнюдь не только один Дункан МакЛауд) живут в среднем намного дольше, но воду пьют не из водопровода - горные реки берут свое начало от ледников, где уровень антропогенных загрязнений минимальный. Итак, какие же параметры определяют качество воды? Для аквариумистов в первую очередь важно содержание аммиака (аммония), нитритов, нитратов, фосфатов, железа, меди и других тяжелых металлов, органических и хлорорганических соединений. Последние обладают очень стойким характерным неприятным запахом, который и позволяет обнаруживать их даже в очень небольших концентрациях. Достаточно просто принюхаться к воде и почувствовать их так сказать органолептически. Если у вас вода из-под крана пахнет "дустом", то не пейте ее сами и не лейте рыбкам без очистки. Очищать ее можно пропуская через фильтр с активированным углем. Оценить степень загрязненности воды органическими веществами можно по показателю ее окисляемости и редокс потенциалу (Rh). Для определения многих, перечисленных выше загрязнителей существуют различные тесты от разных фирм (УВАЖАЕМЫЕ ФИРМЫ-ПРОИЗВОДИТЕЛИ И ДИСТРИБЬЮТЕРЫ!!! ЗДЕСЬ МОГЛА БЫ БЫТЬ ВАША РЕКЛАМА!!!), спрашивайте в зоомагазинах. Вообще то, оценить качество водопроводной воды с помощью ограниченного набора тестов удается не всегда, хотя если чувствуете, что с водой что-то не ладно, начинайте именно с них. Дело в том, что в настоящее время существует огромное количество различных загрязнителей (токсичных примесей), которые в принципе могут быть обнаружены в водопроводной и аквариумной воде. По оценкам одних авторов их СОТНИ ТЫСЯЧ, а по оценкам других - только ДЕСЯТКИ ТЫСЯЧ (от этого не легче, правда?). Невозможно обзавестись тестами на все возможные загрязнители, и жизни не хватит, чтобы выполнить все анализы. К тому же, в различных сочетаниях вещества-загрязнители могут оказывать либо более слабое, либо более сильное токсическое действие, которое может проявляться даже если их содержание воде не превышает ПДК. В этом случае оценить качество воды можно с помощью методов биотестирования, выявляющих так называемую ОБЩУЮ ТОКСИЧНОСТЬ. С помощью биотестов, например, можно установить выделяют ли пластмассовые элементы оформления аквариума в воду вредные вещества, или же они поступают из водопровода. Но это уже отдельная серьезная и большая тема. Будет время - напишу. Следите за нашими обновлениями на главной странице! В. Ковалёв, кандидат биологических наук. * Г.Й.Майланд "Аквариум и его обитатели", БММ АО, Москва 1998. **См., например, К.Кассельман "Атлас аквариумных растений", 2 издание, Москва "Аквариум", 2001. © Живая Вода Сообщение отредактировал akvamistika - 23.11.2008, 22:33 » Спасибо сказали: «
|
| Necromancer |
 15.11.2008, 20:43 15.11.2008, 20:43
Сообщение
#3
|
 Болтун  Куратор темы Сообщений: 525 Регистрация: 21.3.2008 Из: Новосиб - Барнаул Пользователь №: 26 086 Репутация:  99 99  |
Углекислый газ и активная реакция воды. Или как сделать так, чтобы на листьях аквариумных растений не росли сталагмиты О том, зачем и как надо управлять содержанием углекислого газа в аквариуме. » Спойлер (нажмите, чтобы прочесть) « Известно, что углекислый газ жизненно необходим растениям. Ассимилированный в ходе процесса фотосинтеза СО2 является основным строительным материалом для синтеза органических молекул. И аквариумные растения тут не исключение. При дефиците углекислого газа им будет просто не из чего строить свои ткани, что сильно замедлит или совсем прекратит их рост. С другой стороны, при избытке углекислоты в воде аквариума рыбы начинают задыхаться даже тогда, когда содержание в ней кислорода велико (Эффект Рута). Следовательно аквариумист, если только он хочет любоваться живыми, а не пластмассовыми растениями и рыбами, должен уметь поддерживать концентрацию углекислого газа в воде в оптимальном диапазоне.
С достаточной точностью аквариумист-любитель может определить содержание углекислоты в воде аквариума расчетным путем, если он знает величину показателя рН и карбонатную жесткость воды, о чём и будет рассказано в настоящей статье. Но сначала надо дать ответ на такой вопрос: а надо ли вообще аквариумисту что-то измерять и затем что-то рассчитывать? Так ли уж необходимо "проверять алгеброй гармонию"? Ведь всё в природе способно к саморегуляции. Аквариум – это тоже по сути своей маленький "кусочек" природы и он не представляет собой исключения из этого правила. В аквариуме нормальных (классических) пропорций* с достаточным, но не большим количеством рыб, нужные параметры воды обычно устанавливаются сами собой. Чтобы в дальнейшем они не отклонялись от нормы, надо не перекармливать рыбу, регулярно и не реже, чем раз в две недели подменивать примерно четверть или треть объёма воды. И этого действительно будет достаточно. Рыбы в ходе своей жизнедеятельности выделяют достаточное количество углекислоты, нитратов и фосфатов для того, чтобы растения не бедствовали. В свою очередь растения обеспечивают рыб достаточным количеством кислорода. Начиная с последней четверти IXX века (со времён Н.Ф. Золотницкого) и на протяжении большей части века XX так поступали почти все аквариумисты. Всё у них было хорошо, а что такое аквариумные тесты многие из них вообще не знали… Современная же аквариумистика без использования средств определения параметров аквариумной воды просто немыслима. Что же изменилось? Технические возможности! С помощью специального оборудования мы стали обманывать природу. В маленькой стеклянной коробочке, которую по сути представляет собой типичный комнатный аквариум (а даже солидный для комнатного водоёма объем в 200-300 л сравнительно с природным водоемом очень мал) появилась возможность содержать такое количество живых организмов, которое никак не соизмеримо с естественными ресурсами в ней имеющимися. К примеру, в совершенно неподвижной и ничем не перемешиваемой воде аквариума у самой его поверхности на глубине 0.5-1 мм количество кислорода может быть вдвое большим, чем на глубине всего только нескольких сантиметров. Переход кислорода из воздуха в воду сам по себе происходит очень медленно. По вычислениям некоторых исследователей, молекула кислорода в силу одной лишь диффузии за сутки может углубиться не более чем на 2 см! Поэтому без технических средств, перемешивающих или аэрирующих воду, аквариумисту просто невозможно заселить аквариум "лишними" рыбами. Современное аквариумное оборудование позволяет посадить в аквариум и некоторое время успешно содержать в нем немыслимое по прежнем временам количество рыб, а яркие лампы очень плотно засадить аквариум растениями и даже покрыть его дно густым слоем ричии!  Это фрагмент дна аквариума. Оно плотно засажено почвопокровными растениями: глоссостигмой (Glossostigma elatinoides), яванским мхом (Vesicularia dubyana) и риччией (Riccia fluitans). Последняя обычно плавает у поверхности, но можно добиться того, чтобы она росла на дне. Для этого аквариум нужно ярко освещать и подавать в воду углекислый газ. Креветка Амано тоже не случайно попала в кадр, надо же кому аккуратно и бережно выбирать остатки корма из гущи рогулек Но нельзя забывать, что обманутая природа с того самого мига, как мы сверхплотно заселили аквариум живыми организмами ни за что больше уже не отвечает! Устойчивая жизнеспособность такой системы теперь отнюдь не гарантирована. За тот экологический беспредел, который аквариумист устроил в своём аквариуме, в ответе будет он и только он. Даже незначительная его ошибка приведет к экологической катастрофе. А чтобы не ошибаться надо знать как и почему изменяются хотя бы основные параметры воды. Своевременно их контролируя можно оперативно вмешиваться в работу перенаселенной и потому нестабильной системы, снабжая её недостающими ресурсами и удаляя избыточные отходы, которые аквариумный "биоценоз" сам не способен утилизировать. Одним из таких необходимых для аквариума с живыми растениями ресурсом является углекислый газ.  Снимок сделан на семинаре, проведенном Такаси Амано в Москве в 2003 г. Это вид аквариума сзади. Искусственный задний фон здесь не предусмотрен. Его создадут растения, чрезвычайно плотно высаженные вдоль задней стенки. Для того, чтобы они могли вырасти не "задушив" друг друга использовано сразу несколько хитростей, основанных на аквариумных высоких технологиях. Это специальный многослойный не закисающий грунт, богатый доступными для растений минеральными веществами, очень яркий источник света со специально подобранным спектром, и конечно же устройство, обогащающее воду CO2 (все произведено фирмой ADA)  Часть системы, обогащающей воду аквариума углекислотой крупным планом. Снаружи крепится устройство, позволяющее визуально контролировать подачу пузырьков газа в аквариум. Внутри расположен диффузор. Для наглядности, устроители семинара пустили газ очень сильно и от диффузора поднимается целый столб пузырьков. Столько углекислого газа аквариумным растениям не надо. В режиме нормальной работы, когда газа подается гораздо меньше, пузырьков почти не должно быть видно, так как углекислый газ быстро растворяется в воде. Таким образом, буйная растительность в "природном" аквариуме Такаси Амано не растет сама собой – для этого требуется специальное оборудование. Так что не такой уж этот аквариум "природный", он скорее техногенный! В атмосфере земли СО2 очень немного – всего 0.03%. В сухом атмосферном воздухе при стандартном барометрическом давлении (760 мм. рт. ст.) его парциальное давление составляет всего 0.2 мм. рт. ст. (0.03% от 760). Но и этого очень незначительного количества вполне достаточно, чтобы он значимым для аквариумиста образом обозначил своё присутствие. К примеру, дистиллированная или хорошо обессоленная вода, постояв в открытой таре достаточное время для того чтобы успеть прийти в равновесие с атмосферным воздухом**, станет слегка кислой. Это произойдет потому, что в ней растворится углекислый газ. При указанном выше парциальном давлении углекислого газа его концентрация в воде может достичь 0.6 мг в л, что приведет к падению рН до значений близких к 5.6. Почему? Дело в том, что некоторые молекулы углекислого газа (не более 0.6%) взаимодействуют с молекулами воды с образованием угольной кислоты: CO2+H2O <–> H2CO3 Угольная кислота диссоциирует на ион водорода и гидрокарбонатный ион: H2CO3 <–> H+ + HCO3- Этого оказывается достаточно для подкисления дистиллированной воды. Напомним, что показатель рН (активная реакция воды) как раз и отражает содержание ионов водорода в воде. Это отрицательный логарифм их концентрации. В природе точно также подкисляются капли дождя. Поэтому даже в экологически чистых регионах, в которых в дождевой воде нет серной и азотной кислот, она все равно слегка кислая. Проходя затем через почву, где содержание углекислого газа во много раз выше, чем в атмосфере, вода еще больше насыщается углекислотой. Взаимодействуя затем с породами, содержащими известняк, такая вода переводит карбонаты в хорошо растворимые гидрокарбонаты: CaCO3 + H2O + CO2 <–> Ca(HCO3)2 Эта реакция обратима. Она может быть смещена в право или влево в зависимости от концентрации углекислого газа. Если содержание СО2 достаточно продолжительное время остается стабильным, то в такой воде устанавливается углекислотно-известковое равновесие: новых гидрокарбонатных ионов не образуется. Если тем или иным способом убрать СО2 из равновесной системы, то она сдвинется влево, и из раствора, содержащего гидрокарбонаты выпадет в виде осадка практически нерастворимый карбонат кальция. Так происходит, например, при кипячении воды (это известный способ снижения карбонатной жесткости, то есть концентрации в воде Ca(HCO3)2 и Mg(HCO3)2). Этот же процесс наблюдается и при простом отстаивании артезианской воды, которая под землёй находилась при повышенном давлении и там в ней растворилось много углекислоты. Оказавшись на поверхности, где парциальное давление СО2 мало, эта вода отдает лишний углекислый газ в атмосферу до тех пор пока не придет с ней в равновесие. При этом в ней появляется беловатая муть, состоящая из частичек известняка. Точно по такому же принципу образуются сталактиты и сталагмиты: сочащаяся из подземных пластов вода освобождается от лишней углекислоты и одновременно от карбонатов кальция и магния. И по сути эта же реакция происходит на листьях многих аквариумных растений, когда они активно фотосинтезируют на ярком свету, а углекислый газ в замкнутом пространстве аквариума заканчивается. Вот тут их листья начинают "седеть", так как они покрываются корочкой карбоната кальция (об этом рассказано поподробнее в другой статье). Но раз из воды извлекается вся свободная углекислота, то и рН при этом неумолимо растёт. Обычно растения могут поднять рН аквариумной воды до 8.3-8.5. При таком показателе активной реакции воды в ней почти совсем нет молекул углекислого газа и растения (те виды, что умеют это делать, а умеют многие) занимаются добычей углекислоты из бикарбонатов. Ca(HCO3)2 –> CO2 (поглощается растением) + CaCO3 + H2O Как правило, они не могут поднять рН еще выше, так как его дальнейший рост сильно ухудшает функциональное состояние самих растений: фотосинтез, а следовательно изъятие СО2 из системы замедляется, и находящийся в воздухе углекислый газ, растворяясь в воде, стабилизирует рН. Аквариумные растения, таким образом, могут буквально душить друг друга. Выигрывают те виды, что лучше извлекают углекислоту из гидрокарбонатов, а страдают не умеющие это делать, к примеру, роталы и апоногетоны мадагаскарской группы. Именно такие растения считаются у аквариумистов самыми нежными.  Водные растения в этом аквариуме не в лучшем состоянии. Долгое время он существовал в условиях острого дефицита углекислого газа, затем была организована его подача. Результаты очевидны. Свежая зелень макушек говорит сама за себя. Особенно сильно эффект подачи углекислоты заметен на роталах (Rotala macrandra). Они почти погибли, о чем свидетельствуют почти полностью лишенные листьев нижние участки стеблей, но ожили и дали красивые красноватые листья, очень быстро выросшие уже во время подачи газа Те растения, что могут расщеплять гидрокарбонаты более живучи. К таковым относят рдесты, валлиснерию, эхинодорусы. Однако густые заросли элодеи способны и их задушить. Элодея может еще эффективнее извлекать связанную в гидрокарбонатах углекислоту: Ca(HCO3)2 –> 2CO2(поглощается растением) + Ca(OH)2 Если карбонатная жесткость воды достаточно велика, то этот процесс может привести к опасному не только для других растений, но и для подавляющего большинства аквариумных рыб росту значения рН аквариумной воды до 10. В аквариумной воде с высокими значениями рН невозможно выращивание целого ряда растений, да и очень многим видам аквариумных рыб щелочная вода определенно не нравится. Можно ли исправить положение усилив аэрацию аквариума в расчете на то, что благодаря высокой растворимости углекислого газа вода аквариума обогатится СО2? Действительно, при нормальном атмосферном давлении и температуре 20°С в одном литре воды могло бы растворится 1.7 г углекислоты. Но это произошло бы только в том случае, если бы газовая фаза с которой соприкасалась эта вода целиком состояла бы из СО2. А, при контакте с атмосферным воздухом, в котором содержится всего 0.03% СО2 в 1 л воды может перейти из этого воздуха только 0.6 мг – это и есть равновесная концентрация, соответствующая парциальному давлению углекислого газа в атмосфере на уровне моря. Если содержание углекислоты в аквариумной воде ниже, то аэрация действительно его поднимет до концентрации 0.6 мг/л и не более! Но обычно содержание углекислого газа в воде аквариума все же выше указанной величины и аэрация приведет лишь к потере СО2. Проблему можно решить искусственно подавая в аквариум углекислый газ, тем более, что это отнюдь не сложно. В этом деле можно обойтись даже без фирменного оборудования, а просто воспользоваться процессами спиртового брожения в сахарном растворе с дрожжами и некоторыми другими крайне нехитрыми устройствами, о которых мы вскоре расскажем. Тут, однако, надо отдавать себе отчет в том, что этим мы обманываем природу ещё раз. Бездумное насыщение воды аквариума углекислым газом ни к чему хорошему не приведет. Так можно быстро уморить рыб, а затем и растения. Процесс подачи углекислоты должен находиться под строгим контролем. Установлено, что для рыб концентрация СО2 в воде аквариума не должна превышать 30 мг/л. А в целом ряде случаев эта величина должна быть хотя бы ещё на треть меньше. Вспомним, что и сильные колебания величины рН для рыб также вредны, а дополнительная подача углекислого газа быстро закисляет воду. Как оценить содержание СО2 и добиться того, чтобы при насыщении воды этим газом значения рН колебались незначительно и оставались в приемлемом для рыб диапазоне? Тут нам будет не обойтись без формул и математических расчетов: гидрохимия аквариумной воды, увы, тема довольно "сухая". Взаимосвязь между концентрациями в воде пресноводного аквариума углекислого газа, ионов водорода и гидрокарбонатных ионов отражает уравнение Хендерсона-Хассельбаха, которое применительно к нашему случаю будет иметь вид: [H+] [HCO3-]/[H2CO3+СО2] = K1 (1) где К1 – кажущаяся константа диссоциации угольной кислоты по первой ступени, учитывающая равновесие ионов со всем количеством углекислого газа в воде – общей аналитически определяемой углекислотой (то есть, как просто растворенными молекулами СО2, так и гидратированными молекулами в форме угольной кислоты - Н2СО3). Для температуры 25°С эта константа равна 4.5*10-7. Квадратные скобки обозначают молярные концентрации. Преобразование формулы даёт: Величины рН и [HCO3-] можно определить с помощью стандартных аквариумных тестов. Следует отметить, что KH-тест определяет именно содержание гидрокарбонатных ионов в воде (а не ионов кальция) и подходит для наших целей. Единственное неудобство его использования связано с необходимостью пересчитывать градусы в М, что, впрочем, вовсе не сложно. Для этого достаточно величину карбонатной жесткости, полученную после выполнения процедуры тестирования в градусах, разделить на 2.804. Концентрацию ионов водорода, выраженную в рН также надо перевести в М, для этого надо 10 возвести в степень равную величине рН с отрицательным знаком: 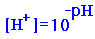 Для перевода рассчитанной по формуле (2) величины [H2CO3 + СО2] из М в мг/л СО2 надо умножить её на 44000. С помощью уравнения Хендерсона-Хассельбаха можно рассчитать концентрацию общей аналитически определяемой углекислоты в аквариуме в том случае, если для стабилизации рН аквариумист не использовал специальных реактивов и содержание гуминовых и прочих органических кислот в его аквариуме умеренное (с достаточной для любителя степенью точности об этом можно судить по цвету аквариумной воды: если она не похожа на "чёрные воды" Амазонии, бесцветна или окрашена только чуть-чуть - значит их там немного). Те, кто на короткой ноге с компьютером, в частности с электронными таблицами Exel, могут на основе приведенной выше формулы и величины К1 составить подробные таблицы, отражающие содержание углекислоты в зависимости от карбонатной жесткости и рН. Мы же приведем тут сокращенный, но, надеемся, полезный для аквариумистов-любителей вариант такой таблицы и калькулятор, позволяющий тут же автоматически рассчитать содержание углекислого газа в воде: Минимальные значения рН воды в аквариуме для заданной карбонатной жесткости, при которых содержание углекислоты еще не опасно для рыб (красные цифры в столбцах), и максимально допустимые величины рН при которых у растений, не умеющих добывать углекислоту из гидрокарбонатов ещё достаточно эффективно идёт фотосинтез (зелёные цифры в столбцах). Для 25°С. 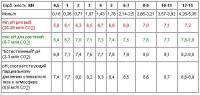 Если вы решили подавать углекислый газ в аквариум, то отрегулируйте его подачу так, чтобы величины рН для соответствующей карбонатной жесткости попадали в интервал между красными и зелеными цифрами. В ходе светового дня активная реакция воды будет изменяться (обычно рН повышается) и это обстоятельство надо учесть при настройке оборудования. Пытайтесь настроиться на середину интервала, тогда величина рН скорее всего не выскочит за его границы. Если подача СО2 регулируется рН-контроллером, перекрывающим подачу газа при снижении рН до заранее заданного уровня, то этот уровень не должен быть ниже минимально допустимого для рыб. Использование рН-контроллера наиболее эффективно и безопасно, но сам он стоит относительно дорого.  На переднем плане этой фотографии еще одна ротала (Rotala wallichii). Слева - маяка речная (Mayaca fluviatilis). Она тоже любительница свободного углекислого газа в воде. При подходящем освещении и содержании углекислоты в аквариуме порядка 15-20 мг/л эти водные растения покрывается пузырьками кислорода, настолько эффективно идет фотосинтез Кроме того, подкормить растения СО2 можно с помощью специальных таблеток, помещаемых в аквариум в особом устройстве. Они постепенно отдают в воду углекислоту. С этой же целью можно в начале светового дня подливать в аквариум слабоминерализованную газированную воду (естественно без пищевых добавок!). Приведенные в этой статье таблица и калькулятор помогут оценить насколько эти меры эффективны. В таблице также указаны величины рН, которые при заданной карбонатной жесткости приобретает хорошо аэрируемая вода в комнатном аквариуме, в том случае если он умеренно заселен рыбами и если окисляемость воды в нём не высока. Иными словами, если подача углекислоты в аквариум вдруг прекратится, то можно ожидать, что рН воды в течение нескольких часов возрастет примерно до этих величин. Цифры в последней строке этой таблицы – это рН воды заданной карбонатной жесткости находящейся в равновесии с атмосферой. Видно, что они еще выше. В природных водоемах, в порогах чистых рек, где вода бурлит и отдает в атмосферу весь лишний (неравновесный) углекислый газ, такие значения рН действительно имеют место. В помещениях же и парциальное давление углекислоты в воздухе выше, чем на открытом воздухе, и процессы, идущие в грунте и фильтре аквариума приводят к образованию углекислого газа и ионов водорода. Всё это обеспечивает большее, чем в естественных условиях содержание углекислоты в воде аквариумов и вода в них при той же карбонатной жесткости оказывается более кислой. Теперь обратим внимание на такой факт. Угольная кислота, которая образуется при растворении атмосферного углекислого газа в воде снижает рН дистиллированной воды до 5.6, а вода с карбонатной жесткостью, к примеру, равной 5 kH, находясь в равновесии с атмосферными газами, имеет активную реакцию 8.4. Легко прослеживается такая закономерность: чем выше карбонатная жесткость воды, тем она более щелочная. Вообще-то это правило известно многим, но не все аквариумисты отдают себе отчёт в том, что речь идет именно о карбонатной жесткости. Действительно, если иметь дело только с природными пресными водами, в которых карбонатная жесткость, как правило, вносит весьма значительный вклад в общую, об этом можно и не задумываться, но вот в искусственно приготовленной воде все может быть по-другому. Например, добавление хлористого кальция поднимет жесткость воды, но не рН. То, что природные воды обычно имеют слабощелочную активную реакцию связано именно с наличием в них гидрокарбонатных ионов. Вместе с растворенной в воде углекислотой, они образуют углекислотно-гидрокарбонатную буферную систему, которая тем сильнее стабилизирует рН воды в области щелочных значений, чем выше концентрация гидрокарбонатов (карбонатная жесткость). Чтобы понять почему так происходит и выбрать оптимальные для аквариума значения карбонатной жесткости надо снова обратиться к формуле Хендерсона-Хассельбаха, но сделаем мы это в следующий раз. Продолжение следует. В. Ковалёв, Е. Ковалёва, фото авторов. 30 января 2005 г. *Классические пропорции аквариума таковы: ширина равна или не более чем на четверть меньше высоты. Высота не превышает 50 см. Длинна же, в принципе, не ограничена. В качестве примера можно привести аквариум длинной 1 м, шириной 40 см и высотой 50 см. Биологическое равновесие в таком комнатном водоёме установится относительно легко. Назад к тексту **Под равновесием с атмосферным воздухом мы понимаем такое состояние воды, когда концентрации (напряжения) растворенных в ней газов соответствуют парциальным давлениям этих газов в атмосфере. Если давление какого-либо газа уменьшится, то молекулы этого газа начнут покидать воду, до тех пор пока снова не будет достигнута равновесная концентрация. И наоборот, если парциальное давление газа над водой увеличится, то большее количество этого газа растворится в воде. © Живая Вода Сообщение отредактировал akvamistika - 23.11.2008, 22:31 |
| DizeL |
 16.11.2008, 11:07 16.11.2008, 11:07
Сообщение
#4
|
 Поддерживает разговор  Группа: Sibnet-club Сообщений: 124 Регистрация: 4.11.2007 Из: Барнаул Пользователь №: 9 522 Репутация:  22 22  |
В связи с этим вопрос!!! Для подмены водя использую водопроводную воду, в которую добавляю AquaSafe. Может быть просто поставить фильтр на кран и использовать отфильтрованную воду? Или Барнаульский водоканал дает достаточного качества воду и возможно не стоит применять кондиционеры?
|
| Necromancer |
 16.11.2008, 20:09 16.11.2008, 20:09
Сообщение
#5
|
 Болтун  Куратор темы Сообщений: 525 Регистрация: 21.3.2008 Из: Новосиб - Барнаул Пользователь №: 26 086 Репутация:  99 99  |
В связи с этим вопрос!!! Для подмены водя использую водопроводную воду, в которую добавляю AquaSafe. Может быть просто поставить фильтр на кран и использовать отфильтрованную воду? Или Барнаульский водоканал дает достаточного качества воду и возможно не стоит применять кондиционеры? Я всегда воду фильтрую и потом в течении суток отстаиваю, чтобы излишки кислорода удалить (если требуется подмена большого кол-ва воды, если же объем доливаемой в аквариум воды не превышает 10-15%, то лью просто фильтрованную, не отстаивая). Вода получается весьма качественная (во всяком случае, ни рыбки, ни травки пока не жаловались » Спасибо сказали: «
|
| DizeL |
 17.11.2008, 20:03 17.11.2008, 20:03
Сообщение
#6
|
 Поддерживает разговор  Группа: Sibnet-club Сообщений: 124 Регистрация: 4.11.2007 Из: Барнаул Пользователь №: 9 522 Репутация:  22 22  |
Кондиционерами не пользуюсь, ибо не только не вижу в них смысла при подходе, описанном выше, но и сомневаюсь в их безопасности и полезности для аквариумных обитателей. Смысл есть, он связывает металлы и хлорку. Когда добавляю, запах хлорки исчезает |
| n0ne |
 17.11.2008, 21:50 17.11.2008, 21:50
Сообщение
#7
|
|
Молчун  Группа: Пользователи Сообщений: 77 Регистрация: 8.4.2008 Пользователь №: 28 658 Репутация:  2 2  |
Как Вы понимаете, что вода хорошая, делаете тесты или какие то приметы есть?
При объеме до 100 литров желательно только отстаивать, свыше 100 можно смело лить из крана, не более 40% если больше надо подменить, то лучше сделать это за два этапа. А вообще смеряйти воду из крана и в аквариуме и Вы поймете, что для нашего г.Барнаула вода почти идеальна аквариумных рыб. А если еще учесть, что Вы держите не порвое поколение и даже не второе, а тысяча дцатое, то рыба уже адаптирована к нашим условия. Другое дело когда рыба дикая. Даже в этом случаи имею дикую рыбу и так же лью воду из крана и без каких либо проблем. Рыба нерестится, а это показатель. А вот лишняя химия в аквариумах всегда пагубно складывается на обитателях. Тем более тут писал кто-то что жарил астронотуса, так вот после химии рыбу вообще не рекомендуется употреблять в пищу, это так к слову. |
| Necromancer |
 18.11.2008, 23:50 18.11.2008, 23:50
Сообщение
#8
|
 Болтун  Куратор темы Сообщений: 525 Регистрация: 21.3.2008 Из: Новосиб - Барнаул Пользователь №: 26 086 Репутация:  99 99  |
Смысл есть, он связывает металлы и хлорку. Когда добавляю, запах хлорки исчезает После качественного фильтра, ИМХО, смысла в кондишене нет. Хлор-то связать этот кондиционер может и свяжет, а вот металлы... Большие у меня сомнения в этом... Плюс, связанные вещества все -равно остаются в воде, что, в любом случае, не есть хорошо. |
| Necromancer |
 19.11.2008, 0:05 19.11.2008, 0:05
Сообщение
#9
|
 Болтун  Куратор темы Сообщений: 525 Регистрация: 21.3.2008 Из: Новосиб - Барнаул Пользователь №: 26 086 Репутация:  99 99  |
Как Вы понимаете, что вода хорошая, делаете тесты или какие то приметы есть? При объеме до 100 литров желательно только отстаивать, свыше 100 можно смело лить из крана, не более 40% если больше надо подменить, то лучше сделать это за два этапа. А вообще смеряйти воду из крана и в аквариуме и Вы поймете, что для нашего г.Барнаула вода почти идеальна аквариумных рыб. А если еще учесть, что Вы держите не порвое поколение и даже не второе, а тысяча дцатое, то рыба уже адаптирована к нашим условия. Другое дело когда рыба дикая. Даже в этом случаи имею дикую рыбу и так же лью воду из крана и без каких либо проблем. Рыба нерестится, а это показатель. А вот лишняя химия в аквариумах всегда пагубно складывается на обитателях. Тем более тут писал кто-то что жарил астронотуса, так вот после химии рыбу вообще не рекомендуется употреблять в пищу, это так к слову. Я делаю только тесты на pH + в столе где-то завалялся с времен, когда только начинал держать рыб и растения, тест то ли на аммоний, то ли еще на что... Тогда я был начинающим аквариумистом (да я и сейчас себя профи не считаю, если честно |
| akvamistika |
 20.11.2008, 21:55 20.11.2008, 21:55
Сообщение
#10
|
 Аквариумисты Сибири - объеденяйтесь !!!    Группа: VIP Сообщений: 8 900 Регистрация: 28.8.2007 Из: СССР Пользователь №: 4 944 |
О СВОЙСТВАХ ВОДЫ ДЛЯ АКВАРИУМА
» Спойлер (нажмите, чтобы прочесть) « Вовсе не обязательно становиться лимнологом-любителем (лимнология - озероведение, наука о континентальных водоемах), чтобы добиться в аквариумистике достойных результатов. Такие термины как “жесткость воды”, “показатель рН”, “электропроводность” и т.п. мы найдем во всех журналах и книгах, посвященных аквариумистике, а потому мы должны понимать, что они для нас означают. Каждому аквариумисту должна быть известна, по крайне мере, жесткость воды в его домашнем водопроводе. А как узнать иначе, подходящую ли воду он наливает в аквариум для своих питомцев? Вообще-то говоря, можно позвонить на водопроводную станцию и получить общие сведения по этому поводу. В Германии раньше было принято публиковать таблицы с показателями воды в поселках и городах, но теперь и они часто не соответствуют действительности, так как проложены новые водопроводы или введены в действие новые водохранилища. Специализированные магазины предлагают и дешевые, и дорогие принадлежности, реактивы и приборы, с помощью которых можно определить свойства воды в домашних условиях. Жесткость воды В литературе по аквариумистике чаще всего при указании жесткости используют “немецкие градусы жесткости”, обозначая их °dН (реже °dGН). Но читатели литературы на иностранных языках могут встретиться и с другими обозначениями, принятыми в соответствующих странах. Нижеследующая таблица даст вам возможность сравнивать расчеты (по Кlее, дополнено): Единица градуса жесткости (1 °dН) = 10 мг/л окиси кальция (СаО). Соответственно изменению свойств воды при кипячении различают временную и постоянную жесткость. Первая называется карбонатной жесткостью: она состоит из разлагающихся при кипячении гидрокарбонатов кальция и магния. Постоянную жесткость называют также некарбонатной; она вызывается наличием сульфатов кальция и магния и подобных соединений. Карбонатная и некарбонатная жесткость вместе дают общую жесткость. Для определения жесткости воды так, как это обычно делают аквариумисты, нужно использовать упрощенный метод лабораторного тестирования. При этом, правда, можно прийти к результатам, которые, как кажется, не сходятся: выявленная карбонатная жесткость может оказаться выше общей. Дело в том, что при таком упрощенном анализе чаще всего определяется лишь общее содержание солей кальция и магния. Реактивы, с помощью которых можно установить отдельно (!) карбонатную жесткость, определить гидрокарбонаты, в воде выше рН = 8 (какая, например, встречается в трех крупнейших африканских озерах и в регионах Средней Америки) измеряют одновременно и карбонатные ионы, что приводит к другому результату и, кажется, ставит под вопрос проведенный анализ. Другие растворенные в воде соединения, например, бикарбонат натрия, тоже сказываются на измерениях, что, разумеется, приводит к неправильным выводам. Временную жесткость можно устранить с помощью кипячения. А что остается, так это постоянная жесткость, и устранить ее хотя бы отчасти можно только с помощью ионообменника. Такие установки используют для получения мягкой нерестовой воды. В следующей главе будет, в частности, сказано о том, что вода в родных для наших декоративных рыб местах не всегда одинакова. Но жесткая или очень жесткая вода встречается в тропической среде крайне редко. Популярны разговоры о том, что воды Амазонки и ее притоков, как и в Центральной Африке, очень мягки, и даже вода крупных центрально-африканских озер, несмотря на высокий показатель рН, не особенно жесткая! Многие аквариумисты делают из этих разговоров неправильные выводы. А мне, например, удалось установить, что вода в озере Ньяса имеет общую жесткость от 3 до 5° dН, в озере Танганьика - между 7 и 11° dН, а в озере Виктория даже между 1 и 2° dН! Тот, кто не собирается заниматься размножением рыб, вовсе не должен копировать в своем аквариуме экстремальные показатели их родных биотопов. Относительно многих видов можно даже предположить, что они едва ли не лучше себя чувствуют в несколько (!) более жесткой (читай: богатой минеральными солями) воде. Поскольку развитие растений в очень мягкой воде попросту невозможно, для большинства аквариумистов вопрос об этом типе воды не возникает вне зависимости от того, можно его воспроизвести или нет. Определенные рыбы - например, живородящие карпозубые из Центральной Америки - в очень мягкой воде не могут развиваться. В их родных биотопах вода чаще всего богата минеральными солями, кислой никогда не бывает, а бывает чаще всего щелочной. Реакция воды и показатель рН Любые типы воды мы различаем по содержанию кислот и оснований. Показатель рН есть мера содержания кислоты или основания. Ионы в воде являются носителями кислотных или щелочных свойств. Если щелочные и кислотные ионы содержатся в ней в равных количествах, то вода реагирует “нейтрально”, как и происходит (или должно происходить) с дистиллированной водой. В любой воде содержится определенное количество молекул Н2О, разделенных на Н+ - катионы (положительно заряженные ионы водорода) и ОН-анионы (отрицательно заряженные ионы гидроокисла). Общее содержание Н+ и ОН- ионов в литре воды имеет постоянный показатель: 10(-14степень) моль/л (моль - молекулярный вес в граммах, см. также раздел “Новые нормы жесткости”). Поскольку в нейтрально реагирующей воде содержится одинаковое количество ионов Н+ и ОН-, то содержание ионов равно 10(-7степень) моль/л. Итак, нейтральная вода обладает концентрацией водородных ионов 10(-7степень) граммов на литр, то есть в ней содержатся 0,0000001 г Н-ионов и ровно столько же ОН-ионов, Сложно и не наглядно! Это число называют показателем рН (роndus Hydrogenil). Именно для наглядности пишут полностью не его, а только логарифм водородного показателя без отрицательного знака, то есть просто “7”. И соответственно водородный показатель нейтральной среды сокращенно обозначается как “рН 7”. В кислой воде этот показатель ниже, чем 7; в щелочной выше, чем 7. Воды зон умеренного климата обычно дают показатель между 7,5 и 9 - то- есть они (за исключением болотной воды) слегка щелочные. Тропические воды, напротив, обычно имеют показатель рН от 5 до 6,8-то есть более или менее кислы. Разумеется, бывают исключения. Самые известные из таковых - центральноафриканские озера. И хотя река Заир находится от них не так далеко и вода в ней отличается некоторой кислотностью при показателе рН 6,5, в озере Танганьика, например, этот показатель в среднем равен 9,0 (в расположенном южнее озере Ньяcа около 8,4), А в воде небогатого рыбой озера Рудольф на севере показатель рН еще выше: от 9,5 до 10,0. Но даже в знаменитых восточноафриканских натриевых/ натронных/ сульфатных озерах (самое известное из них - Магади) с показателем рН около 11,5 и плотностью раствора от 1,015 до 1,030 (морская вода в аквариуме имеет плотность от 1,020 до 1,028) все-таки живут рыбы (Oreochromis grahami) - прекрасное свидетельство их умения приспосабливаться. Определить показатель рН теперь совсем нетрудно. Промышленность выпускает для аквариумистики специальные индикаторы, с помощью которых установить нужные данные можно без всяких усилий. Эти реактивы продаются в зоомагази-нах. Окраску индикатора, опущенного в аквариумную воду, нужно сравнить с окраской стандартов в цветной шкале. В соответствии с цветом определяется и показатель рН. Мне представляется важным упомянуть и о том, что показатель рН для обессоленной водопроводной воды или природной воды с очень малым содержанием минеральных солей определить крайне трудно. При использовании индикатора (измерение с помощью “листочков рН”) результаты часто оказываются неверными, и опасность ошибки тем больше, чем ниже содержание солей в воде. Полностью обессоленная вода забирает из воздуха углекислоту! Даже самое малое количество углекислого газа оказывает влияние на показатель рН любой воды. Дистиллированная вода в равновесии с углекислым газом при 15° С дает показатель рН = 5,7.Большинство растений хорошо развивается в воде, чей показатель рН находится на нейтральной точке (7.0). При показателях ниже 5,0 и выше 8,5 они чаще всего перестают расти или даже погибают. Электропроводность (микросименс) Отправляясь в путешествие по тропикам, я непременно беру с собой электронный тестер для измерения электропроводности: на свете очень мало вод, чистых настолько, чтобы они не проводили электричество. Но в Южной Америке они мне встречались все-таки довольно часто! Чтобы вода проводила электричество, в ней должны содержаться ионы (электрически заряженные частицы). Электропроводность воды определяет также “осмотическое соотношение” (содержание электролита) в аквариумной воде. Осмотическое давление имеет решающее значение для биологических показателей нерестовой воды. В большинстве случаев размножение рыб удается лишь тогда, когда искусственные условия насколько возможно приближены к естественным. В тропиках, на родине аквариумных рыб, вода чаще всего очень мягкая и бедная минеральными солями. Как уже упоминалось в разделе о жесткости воды, в бассейне Амазонки нередко встречаются столь экстремальные водные показатели, что только удивляешься, как рыбы вообще могут там существовать, - например, при показателе рН 4,5 - 4,9. Как известно, в этой воде живет, в частности, красный неон (Рaracheirodon axelrodi) и вплоть до самых последних лет эту маленькую жемчужину аквариумистики никак не удавалось заставить размножаться в наших условиях, как и некоторые виды расборы из Юго-Восточной Азии. Достигнутые в недавнее время успехи в этой области связаны в первую очередь с научными выводами о взаимосвязи между электропроводностью аквариумной воды и осмотическим давлением. Электропроводность воды измеряется с помощью маленького карманного прибора: транзисторного тестера. Этот прибор стоит относительно недорого и дает заинтересованному аквариумисту точные показания Определять электропроводность следует при 20° С. Если измерение надо провести на открытом воздухе, где нет возможности довести воду до этой температуры, то надо задать действительную температуру. Тогда результат окажется, к примеру, нS26. Температура воды оказывает решающее воздействие на результат. Идеальны для размножения рыб показатели от 25 до 140 нS. О том, что воду можно смешивать с учетом электропроводности, будет подробнее говориться в разделе о нерестовой воде. Но следует подчеркнуть еще раз, что дистиллированная вода хоть и может иметь 0° жесткости, но почти никогда 0 нS электропроводимости. Практика показывает, что градусы проводимости дистиллированной воды всегда достаточно высоки. Если заселить рыб в резервуар, где вода имеет другие показатели, могут возникнуть проблемы. Поэтому при слишком резких изменениях проводности аквариумисты из предосторожности пересаживают производителей постепенно. Таким образом им можно помочь приспособиться к новым жизненным условиям. Сообразно своей природе, рыбы, происходящие из очень бедных минералами вод, для выведения молодняка нуждаются в такой же воде, даже если множество их поколений содержались в воде более жесткой, а значит - богатой минералами. Причина этого - структура рыбьей яйцеклетки. Икринки, как и спермии, состоят из клеток, заключенных в очень тонкую оболочку, так называемую мембрану. Клетки содержат, в частности, воду, а в ней находятся минеральные вещества. Сама икринка тоже окружена водой, и в ней опять-таки растворены минеральные соли. Таким образом, здесь сталкиваются друг с другом два элемента, разделенные одной только упомянутой выше тоненькой мембраной и кажущиеся одинаковыми, но на самом деле зачастую не являющиеся таковыми. Яды в аквариумной воде: циркуляция азота Рыбы обладают пищеварительной системой и выделяют продукты обмена - мочу и кал. Эти субстанции очень скоро растворяются в воде, и методом механической очистки с ними справиться невозможно. Кстати, то же самое происходит и с другими веществами: избыточный или непереваренный корм разлагается, как и необнаруженная мертвая рыба. Это же касается отмерших частей растений. Все это вместе образует органические отходы, включающиеся в циркуляцию, которую не видит глаз, а потому не замечают и многие аквариумисты. В природных водах обычно происходит самоочищение. Предрасполагающими факторами для этого являются, конечно, не очень высокая загруженность воды и богатое содержание кислорода. В разделе, где шла речь о биологических фильтрах, уже упоминались аэробные и анаэробные бактерии. Для требуемого процесса естественного разложения важны первые из названных бактерий - аэробные. Они существуют при наличии кислорода, и с их помощью указанные органические соединения преобразуются в неорганические вещества (углекислота, нитрит, нитрат, сульфат, фосфат и вода). Так называемая циркуляция азота начинается только тогда, когда для работы бактерий создались соответствующие предпосылки. В переводе на язык аквариумистики это означает: нужны обильное аэрирование и циркуляция воды. Аммиак (NНз) - это первая стадия разложения и самый ядовитый из всех продуктов разложения; отвратительно пахнущий газ растворяется в воде и образует щелочь. Чем больше содержание аммиака, тем больше смещение показателя рН в основную область (более 7,0), а также ядовитость воды. Отравления рыб аммиаком принадлежат к числу самых неприятных сюрпризов, которые только может пережить аквариумист. Итак, чем выше показатель рН, тем больше опасность отравления. Есть индикаторы, с чьей помощью можно определять содержание аммиака и держать его таким образом под контролем. Частичная замена воды (в крайнем случае - в несколько заходов) с одновременным осторожным снижением показателя рН устраняет симптомы отравления. Но еще проще содействовать естественным процессам разложения таким образом, чтобы они плавно подвигались вперед (биологический фильтр, если аквариум густо населен). Нитрификацией называется дальнейшее разложение растворенного аммиака особыми бактериями, окисляющими ядовитый аммиак через нитрит (NО2 ) в нитрат (NОз). Эти “специализированные” бактерии (Nitrosomonas иNitrosocоссus) сначала преобразовывают аммиак в нитрит, а потому другая группа бактерий (Nitrobakter и Nitrocystis) обеспечивает окисление нитрита в нитрат. Нитрит ядовит почти так же, как аммиак, а потому содержание нитрита тоже нужно держать под контролем! Если у рыб появились симптомы отравления, нужно также срочно предпринять частичную замену воды. Нитрат - это конечный продукт нитрификации. Удалить его из аквариумной воды трудно, но зато вреден он только в высокой концентрации. При каждой частичной замене вместе со старой водой убирается и нитрат. Но из этого не надо делать вывода, что в водопроводной воде нитрат вовсе не содержится. Попробуйте спросить об этом на водопроводной станции! Нитрат можно удалить из воды с помощью ионообменных смол (см, раздел о воде для размножения рыб). Регулярная частичная смена воды - но как? При смене воды часто делают ошибки, поэтому перед тем как перейти к этой теме, дам вам несколько советов. Во-первых, заливать нужно воду температура и жесткость которой (а по возможности и показатель рН) такие же, как были у воды в аквариуме до начала ее замены. Вообще эта операция нужна для того, чтобы сократить количество продуктов разложения и, главное, сменив воду, снизить содержание конечных продуктов разложения - нитратов. Аквариумисты используют, как правило, воду из водопровода. На любой водопроводной станции есть справочный отдел, где можно получить информацию о ее жесткости, показателе рН, содержании нитратов и, наконец, о содержании хлора. В стадии первичной обработки в воду добавляют в первую очередь хлор и его бактерицидные соединения, а также озон. Сильно хлорированную воду (это достигается, как правило, хлором) всегда отличишь по запаху. Согласно принятым при обработке воды нормам элементарный хлор при показателе рН 6 в воде уже не содержится. В принципе в питьевой воде нашей водопроводной сети не должно быть более 0,3 мг/л активного хлора. Однако опасность хлорирования питьевой воды обычно переоценивают. Хлор улетучивается из воды, когда она сильно движется (фонтанирует, пенится). Поэтому аквариумисту имеет смысл подготовленную для частичной замены новую воду подержать в специальном сосуде (например, пластмассовом бочонке) 1-2 суток, однако если туда поставить аэрирующее устройство, то можно значительно сократить сроки отстаивания. » Спасибо сказали: «
|
| n0ne |
 20.11.2008, 23:25 20.11.2008, 23:25
Сообщение
#11
|
|
Молчун  Группа: Пользователи Сообщений: 77 Регистрация: 8.4.2008 Пользователь №: 28 658 Репутация:  2 2  |
Цитата У мну например, из крана бежит слабокислая жесткая хорошо хлорированная вода... А какой район города? В целом по городу идет вода средней жесткости, что в принципе подходит под обльшое количество рыб. А хлор, что такое хлор, надеюсь химию учили в школе хорошо |
| akvamistika |
 23.11.2008, 22:42 23.11.2008, 22:42
Сообщение
#12
|
 Аквариумисты Сибири - объеденяйтесь !!!    Группа: VIP Сообщений: 8 900 Регистрация: 28.8.2007 Из: СССР Пользователь №: 4 944 |
Понижение жесткоcти воды вымораживанием
» Спойлер (нажмите, чтобы прочесть) « Рыбоводство и Рыболовство Для успешного разведения многих видов рыб совершенно необходима мягrая вода. Так как аквариумист-любитель почти никогда не может достать подходящую по качеству воду из естественных водоемов, он вынужден сам заниматься снижением жесткости воды. Из физических методов для этой цели рекомендуется дистилляция и электролиз, из химических - обработка гашеной известью и щавелевой кислотой. В последние годы стали применять диффузионную обработку воды. Но все эти методы мало пригодны для практического применения в домашних условиях. Для дистилляции и электролиза воды необходима громоздкая аппаратура, которая дорого стоит. Чтобы пользоваться химическими методами, надо обладать специальными знаниями, к тому же и сам процесс очень трудоемок. Поэтому любителя часто постигает неудача. Значит необходим такой метод обработки воды, который будет отвечать следующим требованиям: 1. Он должен быть прост, чтобы любитель мог обходиться минимумом специальных знаний. 2. Нужная аппаратура должна быть дешевой. 3. Процесс обработки воды не должен отнимать у аквариумиста много времени. Этим требованиям удовлетворяет предлагаемый нами метод смягчения воды вымораживанием, который применим, разумеется, только в холодное время года, обычно с ноября по март. Физико-химическая основа этого метода заключается в следующем: при замерзании растворов кристаллизуется чистый растворитель, а раствор насыщается остатком растворенного вещества. Вымерзание чистого растворителя теоретически происходит до тех пер, пока концентрация растворенного вещества в остающемся растворе не достигнет предела растворимости. С этого момента в вымерзающем растворителе присутствует и растворенное вещество. Так происходит процесс очистки жидкости, широко применяемый в химических лабораториях. Водопроводная вода представляет собой раствор жестких составляющих (растворенные вещества) в чистой воде (растворитель). При замораживании такой воды сначала замерзает растворитель, который является почти чистой водой, в то время как жесткие составляющие насыщают раствор. В наших опытах применялась лейпцигская водопроводная вода со средней жесткостью 14 градусов. Вода была заморожена приблизительно до половины объема. Вода, образовавшаяся из растаявшего льда, имела жесткость 2-2.5 градуса. Чем больше поверхность воды, тем лучше она вымораживается. Поэтому надо пользоваться соответствующей посудой. Лучше, если она сделана из синтетических материалов (полихлорвинила, полиэтилена и т.п.), которые лед может деформировать, не разрушая. После того, как вода заморожена до половины или соответствующей части, слой льда пробивают, водный остаток с повышенной жесткостью сливают, а лед растапливают и нагревают. Преимущество описанного метода перед другими заключается в том, что вода при вымораживании не только смягчается, но и опресняется. Тайна нерестовой воды И.Ванюшин г.Мытищи Московской обл. Аквариум 6/2001 » Спойлер (нажмите, чтобы прочесть) « "Советую вам рассказать все без утайки, - сказал я. - Полупризнание хуже, чем запирательство. Кроме того, мы сами уже кое-что знаем." <ALIGN=RIGHT"Этюд в багровых тонах",. А.К.Дойль "Тайна оказалась простой, как репа." <ALIGN=RIGHT"Гиперболоид инженера Гарина", А.Н.Толстой В прежние времена, не имея еще достаточного собственного опыта, я весьма доверчиво относился к советам "бывалых", публикуемым в литературе по аквариумистике. Но многолетняя практика научила меня тому. что слепо следовать даже разумным, на первый взгляд, рекомендациям можно далеко не всегда. Вот лишь несколько примеров. Банальнейший и кочующий из книги в книгу совет: чтобы избавиться от шума микрокомпрессора, нужно поместить его в пенопластовый контейнер и вывесить за окно. Я сделал это, в результате в первую же зиму от холода затвердела и рассыпалась резиновая мембрана воздушного насоса. По методу одного аквариумиста из Прибалтики смастерил гибкий солевой обогреватель - поверьте, очень тщательно и аккуратно. Через два месяца его эксплуатации я получил сильный удар током, так как рекомендованный в заметке кембрик через образовавшиеся микротрещины начал контактировать с аквариумной водой. И т.д., и т.п... Но я не жалею о совершенных по доверчивости ошибках, поскольку считаю, что именно они убедили меня в том. что любой рецепт требует всестороннего осмысления, анализа, жесткой привязки к условиям конкретного аквариумного хозяйства. Мне казалось, что в меня уже намертво впиталось критическое отношение к печатному слову. Тем не менее в 1999 году, узнав из одной статьи. что ее автор при разведении Нурhessobrycon sokolofi использует танин, я заразился этой идеей. С величайшим трудом через знакомых аквариумистов из другого города раздобыл этот редкостный ныне химикат. И что же? Снова нулевой результат. Более того, вода в нерестовике стала портиться с такой скоростью, что пришлось в экстренном порядке принимать меры по спасению производителей. Попереживав какое-то время, я вдруг вспомнил свой столь же неудачный опыт сорокалетней давности, когда танин достать было сравнительно легко, а вот обычного голубого неона, наоборот, очень даже не просто. Популярная аквалитература того времени советовала танин этот добавлять в нерестовую воду непременно, иначе, мол, дело табак! В далеком 1961 году я тоже все препятствия преодолел и танин достал, но результат был тот же, что и сорок лет спустя с "ложной тетрой кровоточащее сердце" - H.sokolofi. Согласитесь, что аквариумистика - забава городская. Ну никак не могу представить себе аквариумиста в деревне, вдохновенно перетаскивающего ведрами колодезную воду, а потом подгоняющего ее (чем Бог послал!) под необходимые параметры для нереста какого-нибудь там красного неона. Если я не прав, прошу прощения у такого сельчанина-аквариумиста и обещаю; попроси он у меня помощи, я не откажу ему в совете - что-нибудь да придумаем. Но вернемся к горожанину. Вот житель мегаполиса прочел, что рыбке требуется торфованная вода или настойка шишек ольхи, а то и того пуще - отвар дубовой коры! Такие советы даются часто и как бы походя. Доверчивый любитель начинает мучиться вопросом: где в городе достать торф, да еще и обязательно какой-то "верховой"! А как выглядит ольха, он вообще не знает. Казалось бы. наиболее естественный выход - купить готовые экстракты в магазине для садоводов или аптеке. Но что за жидкость вам всучат, сказать сложно. В отличие от продуктов питания, состав таких растворов производитель на этикетке обозначать не обязан. А что, если в этот торф для повышения урожая добавили фосфор, серу, еще какую-нибудь нужную сельскохозяйственным культурам, но смертельную для обитателей аквариума химию? А может, это вовсе и не торф, а торфикалий*? (* Торфикалий - человеческие испражнения, подвергшиеся длительному естественному природному разложению (гниению) на "полях орошения" и используемые садоводами в качестве удобрения. Не имеет ничего общего с торфом, но по виду его несколько напоминает.) Напрашивается логичный совет: покупать все "необходимые" добавки можно только в зоомагазинах. О, если бы все было так просто! Возьмем, к примеру, фирменные экстракты торфа. Действительно, жидкость имеет темно-коричневый цвет и окрашивает воду. Но теоретически торф воду должен еще и подкислять, причем весьма чувствительно. В моем распоряжении имеется несколько хороших электронных приборов для определения активной реакции (рН) жидкости. Имею я также и набор эталонных растворов, корректирующих их показания. Поэтому результаты своих измерений вполне обоснованно считаю достоверными. Так вот: во всех фирменных флаконах с торфяной водой, а за время работы на выставке "Мир аквариума" я их много повидал, находится почти нейтральная жидкость, ее рН лишь чуть ниже 7. Я пробовал такой торфяной экстракт и "на язык", поскольку величина рН сама по себе не позволяет определить концентрацию кислоты. Вкус тоже не кислый. Так что хоть весь флакон в аквариум вылей, кислей вода не станет. Не исключено, что в этих растворах используется просто какойто безвредный краситель. Еще хуже обстоят дела с отваром коры дуба (его можно приобрести в аптеке). Но внимательно вчитайтесь в аннотацию. Хранить отвар можно лишь в течение двух суток. А что потом? Потом содержащаяся в нем (а в нашем случае - в аквариумной воде) органика начинает терять свои лечебные свойства, разлагаться, загрязнять воду. С опаскои надо относиться и к рекомендациям по использованию воды из "лесных луж и канав". А вдруг какой-нибудь автолюбитель-путешественник ополоснул в этой лужице свой любимый джип? Я не раз удачно разводил мелких капризных экзотических рыбок и, поверьте, не помню случая, когда бы всерьез потребовался торфяной или какой-то иной экстракт. И не подумайте, пожалуйста, что я этими "торфяными" настойками не пытался помочь своим рыбам. Неоднократно! Но прогресса не заметил. Активная реакция воды после добавки торфяных экстрактов оставалась практически без изменения, жидкость только меняла цвет. Есть две рыбки, достаточно трудные для разведения и требовательные к составу воды, и обе из Южной Америки - дискус и красный неон. Так вот: даже самые авторитетные корифеи от аквариумистики признают, что для этих красавцев лучше, когда вода свободна от любых прославленных добавок (в том числе и фирменного торфяного экстракта). Достаточно, чтобы она была просто чистой и свежей. Они в такой воде нерестятся, а это научно-биологический признак их акклиматизации в неволе. Вместе с тем, живут-то они на своей родине частенько в так называемых "черных водах". где растворено столько минерализованной органики, что вода приобретает коричневый цвет. Вот и думай, аквариумист, хорошо ли им было на воле в "торфованной" воде? Я не без оснований считаю, что вливания разного рода реактивов оправданы лишь в том случае, если с их помощью аквариумист сознательно устанавливает требуемую жесткость и активную реакцию, а это уже из области простой неорганической химии. Рыбы - существа очень выносливые. Они, по сути хозяева нашей планеты (после микробов и грибов), жили в мировом океане уже сотни миллионов лет назад и за это время привыкли переносить всяческие невзгоды. Так что и ваши смелые эксперименты они способны кое-как пережить-перетерпеть. Множество аквариумных рыб. которых вы встречаете в зоомагазинах и на рынках, не предъявляют особых требований к химическому составу воды на период размножения. Часто можно получить некоторое количество молодых рыбок даже в той воде. в которой обитают у вас дома их родители. Некоторым нашим популярным питомцам для нереста больше подходит умягченная вода. Вообще же конкретное рассмотрение оптимальных условий для различных рыб и даже их простое перечисление в одной статье отняло бы у нас слишком много времени и внимания. Я расскажу о наиболее требовательной в отношении нерестовой воды группе рыб отряда хараковндных (Characiformes). Это позволит вам составить достаточно полное представление о тех проблемах, которые приходится решать любителю при разведении своих питомцев. Еще раз обращаю ваше внимание на то, что многие аквариумные рыбы не так капризны. Чаще всего в домашних аквариумах разводят мелких представителей этой группы - 5-10 сантиметров длиной. В большинстве своем это жители южноамериканского континента. Реже встречаются хараковидные Африки. Если у вас нет планов по размножению - смело приобретайте харацинок для своего аквариума: подавляющее большинство рыб этого отряда могут годами жить в достаточно жесткой воде (10-15°dGH) с доброй порцией карбонатов (5-7°dKH). в нейтральной и даже слабощелочной среде (рН=7-7,5). Вода в Москве, к примеру, вполне укладывается в эти параметры. Но во время нереста об•становка меняется. Сам нерест случается и в жесткой воде, даже происходит оплодотворение икринок молоками самца, но дальше икромета у так называемых "проблемных" харацид дело не идет. Половые продукты этих рыб нормально функционируют и жизнеспособны только в пределах достаточно узкого диапазона параметров воды. Есть сведения о том, что в излишне жесткой воде оплодотворенная икринка все же живет 1,5-2 часа, а затем, не выдерживая проникновения внутрь через ее оболочку избытка солей из окружающей среды, гибнет. Однако если успеть вовремя переместить икринки в подходящую более мягкую воду - нормальное развитие продолжится. Очевидно, что без мягкой воды для таких рыб обойтись нельзя. На мой взгляд, рациональным решением проблемы нерестовой воды является применение для ее смягчения ионообменных смол. Любитель получает в свое распоряжение практически обессоленную (деминерализованную) воду в любом требующемся количестве и с высокой скоростью. Так, мои четырехлитровые ионообменные колонки выдают за 5-10 минут 10-12 литров воды жесткостью 0,2-0,3°dGH. В аквариумных справочниках иногда встречаются специальные таблицы, которые помогают любителю смягчить водопроводную воду до нужного уровня добавлением в нее определенного количества дистиллированной. Таблицы эти предполагают, что дистиллированная вода имеет нулевую жесткость. Однако это не так, в ней всегда остается 1-1,5°dGH, а иногда и с долей карбонатов, что зависит от конструкции применявшегося дистиллятора, исходной жесткости перегоняемой воды и аккуратности лаборанта. Отсюда возникают ошибки. Могу предложить решать эту задачку с применением очень простой арифметической формулы. Ответ получается точным, если вы заранее знаете жесткость водопроводной и вашей дистиллированной воды. Эта же формула позволит рассчитать соотношение при смешивании двух вод с разной жесткостью. Q = (H1 - h) / (H2 - h) , где H1 - жесткость исходной воды; Н2 - жесткость воды, которую требуется получить; h - жесткость добавляемой воды; Q - количество частей добавляемой воды к одной части исходной воды; Пример 1. Смягчение воды при H1 = 10, H2 = 4, h = 1: Q = (10 - 1) / (4 - 1) = 9 / 3 = 3 , т.е. к одной части исходной воды надо добавить три части мягкой. Пример 2. Получение более жесткой воды. H1 = 10, H2 = 20, h = 30: Q = (10 - 30) / (20 - 30) = (-20) / (-10) = 2 , т.е. к одной части исходной воды надо добавить две части жесткой. Примечание. Если знаменатель дроби получается больше числителя - задача поставлена неверно (например, если при сливании двух мягких вод вы хотите получить жесткость выше исходной). Табл.1 Количества некоторых солей кальция и магния, соответствующие жесткости в 10° dGH, мг/л Са(НСО3)2 - 29,0 Mg(HCO3)2 - 26,2 СаСО3 - 17,8 МgСО3 - 15,0 CaCI2 - 19,8 MgCI2 - 17,0 CaSO4 - 24,3 MgSO4 - 21,5 CaO - 10,0 MgO - 7,2 Табл.2 Регулирование dNKH с использованием 10%-ного раствора MgSO4 10%-ный раствор MgSO4, мл/л -- получаемая dNKH 0,2 -- 0,56 0,4 -- 1,12 0,6 -- 1,40 0,8 -- 1,96 1,0 -- 2,24 1,2 -- 2,80 1,4 -- З,08 Табл.3 Регулирование dNKH с одновременным использованием 10%-ных растворов MgSO4 и CaSO4 MgSO4, мл/л -- CaSO4, мл/л -- dNKH 0,1 -- 0,1 -- 0,56 0,2 -- 0,2 -- 1,12 0,3 -- 0,3 -- 1,68 0,4 -- 0,4 -- 2,24 0,5 -- 0,3 -- 2,80 0,6 -- 0,6 -- 3,36 0,7 -- 0,7 -- 3,92 Рыбам полезна в нерестовике некарбонатная жесткость (dNKH). которая получается добавкой в дистиллированную воду химически чистых растворимых солей кальция и магния. Если вас не пугает перспектива точного отвешивания химреактивов, можно воспользоваться данными табл.1. Повышение некарбонатной жесткости (dNKG) обессоленной воды удобно осуществлять с помощью 10%-ных растворов MgS04 и CaS04. В их составлении помогут табл. 2 и 3. На практике возможно применение упрощенного дозированного способа. Я им пользуюсь так. В 0,5 литра деминерализованной (дистиллированной) воды растворяю некоторое количество солей кальция и магния в соотношении 2:1, например чайную ложечку MgCl2 и две ложечки CaS04. Часть готового раствора наливаю во флакончик с капельницей. Затем делаю пробу. В один литр деминерализованной (дистиллированной) воды добавляю 10 капель раствора. Измеряю получившуюся жесткость и по этим данным в дальнейшем рассчитываю количество капель, добавляемых в нерестовик (при известном его объеме) для получения нужной некарбонатной жесткости. Так, например, если у вас в литре контрольного раствора получилась жесткость 10°dGH, то для получения 4°dGH надо на каждый литр деминерализованной воды в нерестовике добавить по 4 капли маточного раствора. Если соотношение получается не такое простое, как в моем примере, надо сосчитать, сколько градусов жесткости в литре воды дает одна капля маточного раствора, потом разде- лить величину требующейся жесткости нерестовой воды на полученную величину. В соответствии с результатом и следует добавлять раствор солей из капельницы в нерестовик. Получается сразу точно. Коррекцию активной реакции воды рН следует делать с помощью растворов ортофосфорной кислоты НзР04 (для снижения) и натриевой щелочи NaOH (для повышения). Растворы нужны слабые (5-10%), добавляются они в воду по 2-3 капли, и тут же после тщательного перемешивания проверяется результат. Надо под рукой иметь оба раствора, чтобы случившуюся ошибку передозировки сразу исправить добавкой противоположного раствора, так как их совместное применение допустимо. Можно пользоваться химически чистой серной кислотой в том же порядке, но этот реагент по своей природе более агрессивен и может наделать дырок на вашей одежде. Подготовленная вода должна постоять под продувкой 1-2 дня, чтобы установился нормальный газовый состав (обессоливание воды его резко нарушает). В это же время можно в нерестовик поместить растения, чтобы их выделения несколько "оживили" воду. Для этой цели лучше других почему-то подходит таиландский папоротник (Microsorum pteropus). Все манипуляции с подгонкой параметров воды, разумеется, удобнее и безопаснее проводить до помещения в нерестовик растений и рыб. В заключение - таблица с рекомендуемыми параметрами нерестовой воды для некоторых южноамериканских харацинок. На практике успех иногда приходит и при иных показателях жесткости и активной реакции воды, о чем нередко сообщается в аквариумной литературе, однако рекомендуемые условия все же следует считать наиболее подходящими. Более мягкая вода и особенно отсутствие в ней карбонатов в подавляющем большинстве случаев не оказывают отрицательного воздействия на воспроизводство рыб. Таблица составлена по усредненным данным российских и зарубежных публикаций. Латинские названия рыб расположены по мере увеличения требовательности к общей и карбонатной жесткости. Табл.4 Рекомендуемые значения общей (dGH) и карбонатной (dKH) жесткости нерестовой воды для некоторых харациновых Южной Америки Вид (латинское название) / dGH / dKH Astyanax fasciatus mexicanus, Gymnocorymbus ternetzi, Hyphessobrycon ecuadoriensis (Astyanax sp.) / - / - Prionobrama filigera / до 10 / - Pristella maxillaris / 10 / - Moenkhausia sanctadlomena, M.pittieri / 7-9 / 2 Ctenobrycon spilurus / 7-8 / 3 Hemigrammus armstrongi, H. caudovittatus, H. ocelifer, H. pulcher, H. rodwayi, Hyphessobrycon flammeus, H. sholzei, H. unilineatus / 7 / - Aphiocharax anisitsi, A.rathbuni, Hemigrammus erithrozonus, Hasemania marginata (nana) / 6-8 / 1 Copella arnoldi / 5-6 / 1 Hyphessobrycon callistus, H. ornatus, H. serpae, H.takesi, H. pyrrhonotus, H. rubrostigma, H. socolofi / 5 / 1 Nematobrycon amphiloxus ("черный пальмери"), N. palmeri, N. lacortei / 4-6 / 0,5 Poecilobrycon eques, P. unifasciatus / 4 / 1 Megalamphodus megalopterus, M. roseus, M. sweglesi, Thayeria boehlkei, Hyphessobrycon pulchripinnis, Nannostomus (все виды) / 4 / 0,5 Hyphessobrycon loretoensis, H. metae, H. peruvianus, Paracheirodon innesi, Inpaichthys kerri / 3 / 0,5 Hemigrammus bleheri (rhodostomus), H. hyanuary, Hyphessobrycon amandae, H. herbertaxelrodi, Paracheirodon axelrodi, P. simulans / 1,5-2 / 0 Примечание: прочерк означает, что данный показатель не имеет значения О СВОЙСТВАХ ВОДЫ ДЛЯ АКВАРИУМА » Спойлер (нажмите, чтобы прочесть) « Вовсе не обязательно становиться лимнологом-любителем (лимнология - озероведение, наука о континентальных водоемах), чтобы добиться в аквариумистике достойных результатов. Такие термины как “жесткость воды”, “показатель рН”, “электропроводность” и т.п. мы найдем во всех журналах и книгах, посвященных аквариумистике, а потому мы должны понимать, что они для нас означают. Каждому аквариумисту должна быть известна, по крайне мере, жесткость воды в его домашнем водопроводе. А как узнать иначе, подходящую ли воду он наливает в аквариум для своих питомцев? Вообще-то говоря, можно позвонить на водопроводную станцию и получить общие сведения по этому поводу. В Германии раньше было принято публиковать таблицы с показателями воды в поселках и городах, но теперь и они часто не соответствуют действительности, так как проложены новые водопроводы или введены в действие новые водохранилища. Специализированные магазины предлагают и дешевые, и дорогие принадлежности, реактивы и приборы, с помощью которых можно определить свойства воды в домашних условиях. Жесткость воды В литературе по аквариумистике чаще всего при указании жесткости используют “немецкие градусы жесткости”, обозначая их °dН (реже °dGН). Но читатели литературы на иностранных языках могут встретиться и с другими обозначениями, принятыми в соответствующих странах. Нижеследующая таблица даст вам возможность сравнивать расчеты (по Кlее, дополнено): Единица градуса жесткости (1 °dН) = 10 мг/л окиси кальция (СаО). Соответственно изменению свойств воды при кипячении различают временную и постоянную жесткость. Первая называется карбонатной жесткостью: она состоит из разлагающихся при кипячении гидрокарбонатов кальция и магния. Постоянную жесткость называют также некарбонатной; она вызывается наличием сульфатов кальция и магния и подобных соединений. Карбонатная и некарбонатная жесткость вместе дают общую жесткость. Для определения жесткости воды так, как это обычно делают аквариумисты, нужно использовать упрощенный метод лабораторного тестирования. При этом, правда, можно прийти к результатам, которые, как кажется, не сходятся: выявленная карбонатная жесткость может оказаться выше общей. Дело в том, что при таком упрощенном анализе чаще всего определяется лишь общее содержание солей кальция и магния. Реактивы, с помощью которых можно установить отдельно (!) карбонатную жесткость, определить гидрокарбонаты, в воде выше рН = 8 (какая, например, встречается в трех крупнейших африканских озерах и в регионах Средней Америки) измеряют одновременно и карбонатные ионы, что приводит к другому результату и, кажется, ставит под вопрос проведенный анализ. Другие растворенные в воде соединения, например, бикарбонат натрия, тоже сказываются на измерениях, что, разумеется, приводит к неправильным выводам. Временную жесткость можно устранить с помощью кипячения. А что остается, так это постоянная жесткость, и устранить ее хотя бы отчасти можно только с помощью ионообменника. Такие установки используют для получения мягкой нерестовой воды. В следующей главе будет, в частности, сказано о том, что вода в родных для наших декоративных рыб местах не всегда одинакова. Но жесткая или очень жесткая вода встречается в тропической среде крайне редко. Популярны разговоры о том, что воды Амазонки и ее притоков, как и в Центральной Африке, очень мягки, и даже вода крупных центрально-африканских озер, несмотря на высокий показатель рН, не особенно жесткая! Многие аквариумисты делают из этих разговоров неправильные выводы. А мне, например, удалось установить, что вода в озере Ньяса имеет общую жесткость от 3 до 5° dН, в озере Танганьика - между 7 и 11° dН, а в озере Виктория даже между 1 и 2° dН! Тот, кто не собирается заниматься размножением рыб, вовсе не должен копировать в своем аквариуме экстремальные показатели их родных биотопов. Относительно многих видов можно даже предположить, что они едва ли не лучше себя чувствуют в несколько (!) более жесткой (читай: богатой минеральными солями) воде. Поскольку развитие растений в очень мягкой воде попросту невозможно, для большинства аквариумистов вопрос об этом типе воды не возникает вне зависимости от того, можно его воспроизвести или нет. Определенные рыбы - например, живородящие карпозубые из Центральной Америки - в очень мягкой воде не могут развиваться. В их родных биотопах вода чаще всего богата минеральными солями, кислой никогда не бывает, а бывает чаще всего щелочной. Реакция воды и показатель рН Любые типы воды мы различаем по содержанию кислот и оснований. Показатель рН есть мера содержания кислоты или основания. Ионы в воде являются носителями кислотных или щелочных свойств. Если щелочные и кислотные ионы содержатся в ней в равных количествах, то вода реагирует “нейтрально”, как и происходит (или должно происходить) с дистиллированной водой. В любой воде содержится определенное количество молекул Н2О, разделенных на Н+ - катионы (положительно заряженные ионы водорода) и ОН-анионы (отрицательно заряженные ионы гидроокисла). Общее содержание Н+ и ОН- ионов в литре воды имеет постоянный показатель: 10(-14степень) моль/л (моль - молекулярный вес в граммах, см. также раздел “Новые нормы жесткости”). Поскольку в нейтрально реагирующей воде содержится одинаковое количество ионов Н+ и ОН-, то содержание ионов равно 10(-7степень) моль/л. Итак, нейтральная вода обладает концентрацией водородных ионов 10(-7степень) граммов на литр, то есть в ней содержатся 0,0000001 г Н-ионов и ровно столько же ОН-ионов, Сложно и не наглядно! Это число называют показателем рН (роndus Hydrogenil). Именно для наглядности пишут полностью не его, а только логарифм водородного показателя без отрицательного знака, то есть просто “7”. И соответственно водородный показатель нейтральной среды сокращенно обозначается как “рН 7”. В кислой воде этот показатель ниже, чем 7; в щелочной выше, чем 7. Воды зон умеренного климата обычно дают показатель между 7,5 и 9 - то- есть они (за исключением болотной воды) слегка щелочные. Тропические воды, напротив, обычно имеют показатель рН от 5 до 6,8-то есть более или менее кислы. Разумеется, бывают исключения. Самые известные из таковых - центральноафриканские озера. И хотя река Заир находится от них не так далеко и вода в ней отличается некоторой кислотностью при показателе рН 6,5, в озере Танганьика, например, этот показатель в среднем равен 9,0 (в расположенном южнее озере Ньяcа около 8,4), А в воде небогатого рыбой озера Рудольф на севере показатель рН еще выше: от 9,5 до 10,0. Но даже в знаменитых восточноафриканских натриевых/ натронных/ сульфатных озерах (самое известное из них - Магади) с показателем рН около 11,5 и плотностью раствора от 1,015 до 1,030 (морская вода в аквариуме имеет плотность от 1,020 до 1,028) все-таки живут рыбы (Oreochromis grahami) - прекрасное свидетельство их умения приспосабливаться. Определить показатель рН теперь совсем нетрудно. Промышленность выпускает для аквариумистики специальные индикаторы, с помощью которых установить нужные данные можно без всяких усилий. Эти реактивы продаются в зоомагази-нах. Окраску индикатора, опущенного в аквариумную воду, нужно сравнить с окраской стандартов в цветной шкале. В соответствии с цветом определяется и показатель рН. Мне представляется важным упомянуть и о том, что показатель рН для обессоленной водопроводной воды или природной воды с очень малым содержанием минеральных солей определить крайне трудно. При использовании индикатора (измерение с помощью “листочков рН”) результаты часто оказываются неверными, и опасность ошибки тем больше, чем ниже содержание солей в воде. Полностью обессоленная вода забирает из воздуха углекислоту! Даже самое малое количество углекислого газа оказывает влияние на показатель рН любой воды. Дистиллированная вода в равновесии с углекислым газом при 15° С дает показатель рН = 5,7.Большинство растений хорошо развивается в воде, чей показатель рН находится на нейтральной точке (7.0). При показателях ниже 5,0 и выше 8,5 они чаще всего перестают расти или даже погибают. Электропроводность (микросименс) Отправляясь в путешествие по тропикам, я непременно беру с собой электронный тестер для измерения электропроводности: на свете очень мало вод, чистых настолько, чтобы они не проводили электричество. Но в Южной Америке они мне встречались все-таки довольно часто! Чтобы вода проводила электричество, в ней должны содержаться ионы (электрически заряженные частицы). Электропроводность воды определяет также “осмотическое соотношение” (содержание электролита) в аквариумной воде. Осмотическое давление имеет решающее значение для биологических показателей нерестовой воды. В большинстве случаев размножение рыб удается лишь тогда, когда искусственные условия насколько возможно приближены к естественным. В тропиках, на родине аквариумных рыб, вода чаще всего очень мягкая и бедная минеральными солями. Как уже упоминалось в разделе о жесткости воды, в бассейне Амазонки нередко встречаются столь экстремальные водные показатели, что только удивляешься, как рыбы вообще могут там существовать, - например, при показателе рН 4,5 - 4,9. Как известно, в этой воде живет, в частности, красный неон (Рaracheirodon axelrodi) и вплоть до самых последних лет эту маленькую жемчужину аквариумистики никак не удавалось заставить размножаться в наших условиях, как и некоторые виды расборы из Юго-Восточной Азии. Достигнутые в недавнее время успехи в этой области связаны в первую очередь с научными выводами о взаимосвязи между электропроводностью аквариумной воды и осмотическим давлением. Электропроводность воды измеряется с помощью маленького карманного прибора: транзисторного тестера. Этот прибор стоит относительно недорого и дает заинтересованному аквариумисту точные показания Определять электропроводность следует при 20° С. Если измерение надо провести на открытом воздухе, где нет возможности довести воду до этой температуры, то надо задать действительную температуру. Тогда результат окажется, к примеру, нS26. Температура воды оказывает решающее воздействие на результат. Идеальны для размножения рыб показатели от 25 до 140 нS. О том, что воду можно смешивать с учетом электропроводности, будет подробнее говориться в разделе о нерестовой воде. Но следует подчеркнуть еще раз, что дистиллированная вода хоть и может иметь 0° жесткости, но почти никогда 0 нS электропроводимости. Практика показывает, что градусы проводимости дистиллированной воды всегда достаточно высоки. Если заселить рыб в резервуар, где вода имеет другие показатели, могут возникнуть проблемы. Поэтому при слишком резких изменениях проводности аквариумисты из предосторожности пересаживают производителей постепенно. Таким образом им можно помочь приспособиться к новым жизненным условиям. Сообразно своей природе, рыбы, происходящие из очень бедных минералами вод, для выведения молодняка нуждаются в такой же воде, даже если множество их поколений содержались в воде более жесткой, а значит - богатой минералами. Причина этого - структура рыбьей яйцеклетки. Икринки, как и спермии, состоят из клеток, заключенных в очень тонкую оболочку, так называемую мембрану. Клетки содержат, в частности, воду, а в ней находятся минеральные вещества. Сама икринка тоже окружена водой, и в ней опять-таки растворены минеральные соли. Таким образом, здесь сталкиваются друг с другом два элемента, разделенные одной только упомянутой выше тоненькой мембраной и кажущиеся одинаковыми, но на самом деле зачастую не являющиеся таковыми. Яды в аквариумной воде: циркуляция азота Рыбы обладают пищеварительной системой и выделяют продукты обмена - мочу и кал. Эти субстанции очень скоро растворяются в воде, и методом механической очистки с ними справиться невозможно. Кстати, то же самое происходит и с другими веществами: избыточный или непереваренный корм разлагается, как и необнаруженная мертвая рыба. Это же касается отмерших частей растений. Все это вместе образует органические отходы, включающиеся в циркуляцию, которую не видит глаз, а потому не замечают и многие аквариумисты. В природных водах обычно происходит самоочищение. Предрасполагающими факторами для этого являются, конечно, не очень высокая загруженность воды и богатое содержание кислорода. В разделе, где шла речь о биологических фильтрах, уже упоминались аэробные и анаэробные бактерии. Для требуемого процесса естественного разложения важны первые из названных бактерий - аэробные. Они существуют при наличии кислорода, и с их помощью указанные органические соединения преобразуются в неорганические вещества (углекислота, нитрит, нитрат, сульфат, фосфат и вода). Так называемая циркуляция азота начинается только тогда, когда для работы бактерий создались соответствующие предпосылки. В переводе на язык аквариумистики это означает: нужны обильное аэрирование и циркуляция воды. Аммиак (NНз) - это первая стадия разложения и самый ядовитый из всех продуктов разложения; отвратительно пахнущий газ растворяется в воде и образует щелочь. Чем больше содержание аммиака, тем больше смещение показателя рН в основную область (более 7,0), а также ядовитость воды. Отравления рыб аммиаком принадлежат к числу самых неприятных сюрпризов, которые только может пережить аквариумист. Итак, чем выше показатель рН, тем больше опасность отравления. Есть индикаторы, с чьей помощью можно определять содержание аммиака и держать его таким образом под контролем. Частичная замена воды (в крайнем случае - в несколько заходов) с одновременным осторожным снижением показателя рН устраняет симптомы отравления. Но еще проще содействовать естественным процессам разложения таким образом, чтобы они плавно подвигались вперед (биологический фильтр, если аквариум густо населен). Нитрификацией называется дальнейшее разложение растворенного аммиака особыми бактериями, окисляющими ядовитый аммиак через нитрит (NО2 ) в нитрат (NОз). Эти “специализированные” бактерии (Nitrosomonas иNitrosocоссus) сначала преобразовывают аммиак в нитрит, а потому другая группа бактерий (Nitrobakter и Nitrocystis) обеспечивает окисление нитрита в нитрат. Нитрит ядовит почти так же, как аммиак, а потому содержание нитрита тоже нужно держать под контролем! Если у рыб появились симптомы отравления, нужно также срочно предпринять частичную замену воды. Нитрат - это конечный продукт нитрификации. Удалить его из аквариумной воды трудно, но зато вреден он только в высокой концентрации. При каждой частичной замене вместе со старой водой убирается и нитрат. Но из этого не надо делать вывода, что в водопроводной воде нитрат вовсе не содержится. Попробуйте спросить об этом на водопроводной станции! Нитрат можно удалить из воды с помощью ионообменных смол (см, раздел о воде для размножения рыб). Регулярная частичная смена воды - но как? При смене воды часто делают ошибки, поэтому перед тем как перейти к этой теме, дам вам несколько советов. Во-первых, заливать нужно воду температура и жесткость которой (а по возможности и показатель рН) такие же, как были у воды в аквариуме до начала ее замены. Вообще эта операция нужна для того, чтобы сократить количество продуктов разложения и, главное, сменив воду, снизить содержание конечных продуктов разложения - нитратов. Аквариумисты используют, как правило, воду из водопровода. На любой водопроводной станции есть справочный отдел, где можно получить информацию о ее жесткости, показателе рН, содержании нитратов и, наконец, о содержании хлора. В стадии первичной обработки в воду добавляют в первую очередь хлор и его бактерицидные соединения, а также озон. Сильно хлорированную воду (это достигается, как правило, хлором) всегда отличишь по запаху. Согласно принятым при обработке воды нормам элементарный хлор при показателе рН 6 в воде уже не содержится. В принципе в питьевой воде нашей водопроводной сети не должно быть более 0,3 мг/л активного хлора. Однако опасность хлорирования питьевой воды обычно переоценивают. Хлор улетучивается из воды, когда она сильно движется (фонтанирует, пенится). Поэтому аквариумисту имеет смысл подготовленную для частичной замены новую воду подержать в специальном сосуде (например, пластмассовом бочонке) 1-2 суток, однако если туда поставить аэрирующее устройство, то можно значительно сократить сроки отстаивания. » Спасибо сказали: «
|
| Necromancer |
 11.12.2008, 11:57 11.12.2008, 11:57
Сообщение
#13
|
 Болтун  Куратор темы Сообщений: 525 Регистрация: 21.3.2008 Из: Новосиб - Барнаул Пользователь №: 26 086 Репутация:  99 99  |
Почитала тут о вымораживании... Пишут как жёсткость снизилась, но не указано о временной или постоянной жёсткости идёт речь. Попробую сама морозить и тестировать. Отпишусь что получится Если не ошибаюсь, то вымораживание снижает как временную, так и постоянную жесткость. Цитата Жесткость воды определяется суммарным содержанием в ней растворенных солей кальция и магния. Гидрокарботаны кальция и магния образуют карбонатную или временную жесткость воды, которая полностью устраняется при кипячении воды в течение часа. В процессе кипячения растворимые гидрокарбонаты переходят в нерастворимые карбонаты, выпадающие в виде белого осадка или накипи, с выделением при этом углекислого газа. Соли же сильных кислот, например, сульфаты и хлориды кальция и магния - образуют некарбонатную или постоянную жесткость воды, не изменяющуюся при кипячении воды. Цитата Вымораживание Физико-химическая основа этого метода заключается в следующем: при замерзании растворов кристаллизуется чистый растворитель, а раствор насыщается остатком растворенного вещества. Вымерзание чистого растворителя теоретически происходит до тех пер, пока концентрация растворенного вещества в остающемся растворе не достигнет предела растворимости. С этого момента в вымерзающем растворителе присутствует и растворенное вещество. Так происходит процесс очистки жидкости, широко применяемый в химических лабораториях. Водопроводная вода представляет собой раствор жестких составляющих (растворенные вещества) в чистой воде (растворитель). При замораживании такой воды сначала замерзает растворитель, который является почти чистой водой, в то время как жесткие составляющие насыщают раствор. |
| akvamistika |
 11.12.2008, 14:01 11.12.2008, 14:01
Сообщение
#14
|
 Аквариумисты Сибири - объеденяйтесь !!!    Группа: VIP Сообщений: 8 900 Регистрация: 28.8.2007 Из: СССР Пользователь №: 4 944 |
Почитала тут о вымораживании... Пишут как жёсткость снизилась, но не указано о временной или постоянной жёсткости идёт речь. Попробую сама морозить и тестировать. Отпишусь что получится Одно время не было дистилятора, - приходилось пользоваться этим методом, получается дистилированная вода, - дискусы разводились в ней хорошо. ЗЫ: Если попадется инфа о пользе талой воды - почитайте, очень занимательно. Сообщение отредактировал akvamistika - 11.12.2008, 14:03 |
| akvamistika |
 17.12.2008, 11:37 17.12.2008, 11:37
Сообщение
#15
|
 Аквариумисты Сибири - объеденяйтесь !!!    Группа: VIP Сообщений: 8 900 Регистрация: 28.8.2007 Из: СССР Пользователь №: 4 944 |
Заявления о том что это всё так уж понижает жёсткость - преувеличены. Проблему доставляет как раз постоянная жёсткость, а она не понизилась, Очень большое значение имеет соотношение замерзшей воды к оставшейся, (брал 0.5 - 1 см слой из ведра), что замерзало сверху . Чем больше будет это соотношение, тем более будет повышаться и жесткость. Парамерты воды в то время не замерял, но эффект использования от талой воды - заметен. |
| siriys77 |
 6.3.2009, 19:36 6.3.2009, 19:36
Сообщение
#16
|
 РыБоК люблю большых и маленьких  Группа: Пользователи Сообщений: 1 441 Регистрация: 21.3.2008 Пользователь №: 26 053 Репутация:  592 592  |
Каким должен быть уровень нитратов
В аквариуме не должно быть нулевого уровня нитратов. В подобном случае они могут оказаться лимитирующим фактором роста растений и поглощение мим фосфатов прекратится. Такая ситуация может встретится в сильно заросшем аквариуме (особенно быстрорастущими растениями), при недостаточном количестве рыб. безусловно, нулевой уровень нитратов не означает, что растения их не получают. Он лишь указывает на то, что растения поглощают нитраты (и аммиак/аммоний/нитриты, не дожидаясь их преобразования в нитраты в результате био-фильтрации) с такой же скоростью или быстрее, чем они вырабатываются в системе. Как показывает практика, небольшой уровень нитратов (около 2-5 mg/l) желателен в аквариуме. чтобы была уверенность. что фосфаты являются лимитирующим фактором в росте растений (и водорослей). Обычно, при нулевом уровне нитратов через несколько дней начинается рост уровня фосфатов в воде. При добавлении нитратов - он опять падает до нуля. Если фосфаты на нулевом уровне в аквариуме, то наличие нитратов не вызовет роста водорослей. Следует проверять уровень нитратов, если есть подозрение. что их не хватает. Признаком нехватки нитратов является пожелтение и отмирание старых листьев - они как-бы растворяются в воде (за счет миграции азотных соединений к молодым листьям). В подобном случае следует добавить нитратов - лучше всего KNO3. |
| siriys77 |
 11.3.2009, 23:13 11.3.2009, 23:13
Сообщение
#17
|
 РыБоК люблю большых и маленьких  Группа: Пользователи Сообщений: 1 441 Регистрация: 21.3.2008 Пользователь №: 26 053 Репутация:  592 592  |
Химия воды
Автор: Т.Вершинина, Н.Мешкова, Аквариум 2/1993. » Спойлер (нажмите, чтобы прочесть) « В литературе по аквариумистике часто встречаются выражения: 'жесткая вода', 'мягкая вода'. Что это означает? Жесткость воды - это количество растворенных в ней минеральных солей, в основном солей кальция и магния. Различают общую, или карбонатную, жесткость, и постоянную, или некарбонатную. Общая жесткость равна сумме временной и постоянной жесткости. Измеряется в градусах. В отечественной литературе по аквариумистике приняты немецкие градусы жесткости. Вода с жесткостью от 0 до 4° считается очень мягкой, от 5 до 8° - мягкой, от 9 до 16° - средней жесткости, от 16 до 30° - жесткой, свыше 30° - очень жесткой. Большинство аквариумистов пользуются водопроводной водой, жесткость которой непостоянна и зависит от времени года, количества осадков и географического расположения пункта. Так, в Москве жесткость воды - от 4 до 12°, в Санкт-Петербурге - 2-3°, в Одессе - 12° и выше. Что такое постоянная и временная жесткость? Постоянная (некарбонатная) жесткость зависит от содержания в воде сульфатов и хлоридов кальция и магния, временная (карбонатная) - от содержания бикарбонатов кальция и магния. Первую можно устранить только дистилляцией воды или химическим путем. Как повысить жесткость воды? Если требуется незначительное повышение жесткости воды, в аквариум можно положить куски мрамора (или мраморную крошку). В этом случае она увеличивается медленно, причем чем мягче вода, тем быстрее возрастает ее жесткость. Более удобный и надежный способ - добавление растворов хлористого кальция и сульфата магния (магнезии), продающихся в аптеках. Добавление 1 миллилитра 10-процентного раствора хлористого кальция увеличивает жесткость 1 литра воды примерно на 3°, а добавление 1 миллилитра 25-процентного раствора магнезии - на 4°. Для создания более близкого к природному соотношения ионов кальция и магния рекомендуется использовать одновременно хлористый кальций и магнезию. Как понизить жесткость воды? Есть несколько способов снижения жесткости воды. Простейшие - кипячение и вымораживание. При кипячении в течение 30 минут жесткость снижается почти вдвое, при вымораживании она может снизиться еще сильнее. Для этого воду наливают в неглубокий и полупрозрачный полиэтиленовый таз. После того как половина воды замерзнет (вот почему нужен полупрозрачный таз - удобно следить за процессом замерзания воды), водный остаток, в котором есть соли, сливают, а лед, практически не содержащий солей, растапливают и нагревают воду до нужной температуры. Что такое промилле? Соленость, или минерализация, воды выражается количеством растворенных в ней солей. Их концентрация в граммах на 1 литр называется промилле (°/оо). Что такое показатель рН? Активная реакция водородных ионов (рН) - один из важнейших показателей физико-химического состояния воды. Он определяется количеством содержащихся в воде водородных (Н'1') и гидроксильных (ОН~) ионов. Показатель рН, равный 7, означает нейтральную среду, ниже 7 - кислую, выше 7 - щелочную. Кислотность воды в аквариуме должна соответствовать потребностям рыб и растений. Обычно этот показатель бывает от 6 до 9. Есть рыбы, выносящие значительные колебания величины рН, другие - могут жить только в воде с достаточно стабильной кислотностью. В условиях аквариума показатель рН колеблется даже в течение суток. Это обусловлено биологическими и химическими процессами. Водопроводная вода, отстоявшаяся в течение суток, имеет рН, близкий к нейтральному. Как изменить рН воды в аквариуме? Для изменения рН в воду добавляют кислоту или щелочь. Далеко не все кислоты и щелочи подходят для этой цели. Для подкисления воды в аквариуме лучше всего использовать ортофосфорную кислоту (серная и соляная непригодны). Сначала концентрированную кислоту разбавляют водой (добавляя кислоту к воде, а не наоборот), а затем по каплям вносят в аквариум, контролируя уровень рН. Воду можно подкислять и экстрактом торфа или отваром ольховых шишек. Одну столовую ложку шишек заливают стаканом кипятка и держат на огне 5-7 минут. Когда отвар остынет, его доливают в аквариум из расчета 1 стакан на 10 литров воды. Обычно воду подкисляют только при разведении некоторых видов рыб. В декоративном аквариуме изменять рН не нужно. Для подщелачивания воды любители используют разные щелочи, но мы рекомендуем применять только питьевую соду (гидрокарбонат натрия) из расчета 0,2-0,5 грамма на 1 литр воды. Соду нужно растворить в отдельном сосуде, а затем добавлять в аквариум. Ощелачивание мягкой и очень мягкой воды не дает стойкого результата. В аквариумах, где часть воды регулярно заменяют, рН обычно больше 7, и подщелачивания не требуется. Что такое редокс-потенциал? Редокс-потенциал, или окислительно-восстановительный потенциал - показатель химической и биологической активности воды. Для аквариумиста он имеет значение как показатель насыщенности воды органическими веществами, а проще говоря - загрязненности аквариума. Определяют редокспотенциал при помощи специального электронного прибора - рН-метра. Редокс-потенциал измеряется в условных единицах от 0 до 42. Определить его в домашних условиях, как правило, невозможно. В недавно оборудованном аквариуме он имеет значения 30-34; в нем хорошо растут многие плавающие, а также мелколистные растения со слабой корневой системой (перистолистник, гигрофила, кабомба и др.). Это и может служить показателем высокого редокс-потенциала. Затем постепенно редокс-потенциал снижается. Свидетельство этого - хороший рост эхинодорусов и апоногетонов. В более старом аквариуме, где редокс-потенциал еще ниже, отлично растут криптокорины. Если же и криптокорины начинают чувствовать себя хуже, значит, необходимо чистить грунт, частично заменять веду, устанавливать донный фильтр. Как приготовить экстракт торфа? Отвар торфа готовят следующим образом. В эмалированной посуде вываривают несколько кусков торфа и, остудив, процеживают отвар через вату 2-3 раза. Настой готовят так же, как отвар, но торф не вываривают, а настаивают. На каждые 100 литров воды нужно вносить 0,5-1 литр отвара или настоя. Чтобы наш местный торф по качеству был ближе к тропическому, некоторые аквариумисты добавляют несколько зерен кофе, щепотку чая, лист эвкалипта, а также ольховые шишки и дубовую кору. Отвар или настой добавляют в воду до тех пор, пока она не приобретет светло - янтарный оттенок. Что такое 'старая вода'? В аквариуме постепенно накапливаются продукты жизнедеятельности рыб и растений, которые, разлагаясь, насыщают воду органическими кислотами. При отсутствии фильтра и редкой замене воды этот процесс ускоряется. Вода приобретает желтоватый оттенок и кислую реакцию. Такая вода и называется 'старой'. Какова дозировка компонентов для приготовления торфяной воды? Количество торфа и объем воды, в которой он будет вывариваться, могут быть самыми разными. Не имеет значения, 100 граммов торфа вы взяли или килограмм, в трехлитровой кастрюле варили его или в десятилитровой. Важно, чтобы при добавлении в воду этого отвара она приобрела слабо - янтарный опенок. Концентрированного отвара надо вносить совсем немного, а слабого, жидкого - соответственно больше. Другие компоненты добавляют в очень малых количествах: 4-5 зерен кофе, щепотку чая, 1-2 листа эвкалипта, 4-5 ольховых шишек, 1-2 грамма дубовой коры. |
| siriys77 |
 26.3.2009, 0:16 26.3.2009, 0:16
Сообщение
#18
|
 РыБоК люблю большых и маленьких  Группа: Пользователи Сообщений: 1 441 Регистрация: 21.3.2008 Пользователь №: 26 053 Репутация:  592 592  |
Уровень Ph, общяя жёсткость (GH) и карбонатная жёсткость (KH).
» Спойлер (нажмите, чтобы прочесть) « Если у вас есть аквариум с рыбками, то вы, вероятно, уже немало слышали про важность измерения и регулирования уровня pH, kH и gH в своём аквариуме и в воде, которую вы доливаете в него при частичных подменах… Жизнь рыбы и её благополучие частично определяются водородным показателем pH, карбонатной жёсткостью (kH) и общей жёсткостью (gH) аквариумной воды. Если их показания совпадают с показаниями воды, к которой рыба привыкла, когда жила в природных условиях, то она легко перенесёт жизнь в неволе. Но если эти показания сильно отличаются от тех, в которых рыба родилась и выросла, то вероятнее всего, она долго не проживёт. Многие из нас, начинающих и уже опытных аквариумистов, пользуются тестами для измерения pH, kH и gH. Мы измеряем, меняем их в нужную сторону, но до сих пор не совсем понимаем, что они обозначают и как расшифровываются, не говоря уже о том, как они взаимодействуют и каким образом влияют на рыб! Цель этой статьи - дать понятное определение аббревиатурам pH, kH и gH, в доступной форме объяснить, что они из себя представляют и определить, как они взаимодействуют друг с другом, а также сказать пару слов об их влиянии на жителей аквариума. pH - это водородный показатель среды. Если относительно аквариума, то это показатель кислотности (или щёлочности) воды. pH может быть от 1 до 14. Если мы измерим уровень pH и получим результат от 1 до 7 (например, уксус = ph 2.9 или лимонный сок = ph 2.5) то это говорит о том, что среда кислая (значит, в ней преобладают ионы водорода Н+). Если же мы получили pH от 7 до 14 (например, нашатырный спирт по уровню PH равен 11.5, а кровь человека = ph 7.4) - среда щелочная (значит, в воде преобладают гидроксильные ионы ОН-). Нейтральная среда - когда уровень PH равен 7. Под почти нейтральный ph можно привести в пример такие жидкости как молоко (ph = 6.6 - 6.9) и чистую воду (ph = 7.0). Для удобства шкала делений логарифмична, то есть каждое из показаний (3,6,8,12.. и т.д.) состоит из 10 дополнительных делений. То есть, обычно уровень pH измеряется в целых и десятых. Например, pH чая - 5.5 (пять целых пять десятых), pH пива - 4.5 (четыре целых пять десятых), ph морской воды равен 8.0 (восьми целым), а pH отбеливающей хлорки 12.5 (двенадцать целых пять десятых). Это говорит о том, что пиво - более кислая среда, чем чай. В то время как хлорка - более щелочная по сравнению с морской водой. Помним, что все показатели больше 7.0 - показатели щёлочности. Иногда pH измеряют в целых и сотых (для большей точности). Например, ph крови может быть от 7.36 до 7.44 по шкале современного, более точного измерительного прибора. Большинство пресноводных рыб живёт в воде с уровнем pH от 5,5 до 7,5. Некоторые африканские цихлиды исторически привычны к воде с уровнем Ph 8,4. В силу того, что шкала pH логарифмична, то вариаций баланса воды может быть огромное количество. Есть мнение, что даже малейшее изменение в уровне pH может повлиять на самочувствие и здоровье рыбы не лучшим образом и даже спровоцировать летальный исход. Но на самом деле в природе уровень Ph воды может меняться в течение дня (показания уровня pH утром и вечером совсем неодинаковы), и уж тем более эти показания меняются в зависимости от сезона. Поэтому незначительные изменения не могут негативно повлиять на здоровую рыбу. Но если рыба ослаблена, то последствия бывают разные. Во-первых, изменения pH влияют на дыхательную функцию организма рыб. Чем ниже уровень pH, тем больше в воде содержится кислорода, и, соответственно, чем выше ph (кислая среда), тем меньше кислорода. Также в кислой среде (ph меньше 7) содержится больше CO2, и растения в такой среде растут и развиваются лучше, чем в щелочной (ph выше 7).Как известно, во всём нужна мера. Слишком кислая или чрезвычайно щелочная среда может спровоцировать серьёзные повреждения кожи, жабр и глаз рыбы. Продолжительный контакт со смертоносным уровнем Ph воды может привести к тяжёлому стрессу, усилить выработку слизи и спровоцировать гиперплазию (избыточный рост тканей) и в итоге привести к летальному исходу… Помимо прямых последствий, могут быть и косвенные. При изменении уровня Ph некоторые растворённые в воде компоненты становятся чрезвычайно токсичными. Например, аммиак становится ещё более ядовитым в щелочной среде. Даже колебания ph в пределах нормы для некоторых рыб могут быть очень опасны. Знаете ли вы, что даже у нитрифицирующих бактерий, которые разлагают аммиак на менее токсичные нитриты и нитраты, есть свой предел ph, при котором они справляются со своей задачей и вне которого перестают с ней справляться? При уровне ph 7.5 – 8.6 эти бактерии хорошо работают, но стоит этому уровню начать колебаться ниже или выше, бактерии дают сбой. Изменения ph повлияет и на эффективность лечения или относительную безопасность рыбы при использовании медицинских препаратов во время карантина. Например, хлорамин-Т становится более токсичным при понижении Ph (кислая среда), а вот перманганат калия – наоборот, становится очень ядовитым в щелочной среде. Следите за изменениями уровня ph, и вы всегда будете в курсе того, что происходит в аквариуме, даже если пока этого не видно. Изменения в составе воды сразу же дадут знать, что у вас, например, забился донный фильтр. Как вы это узнаете? Повышенное содержание растворённых в воде отходов ведёт к появлению в воде угольной кислоты, а тот в свою очередь подкисляет воду и понижает уровень ph. Конечно, через пару недель вы это и так поймёте по запаху и цвету воды, и тогда проблем будет куда больше. Подбирая рыб в свой аквариум, руководствуйтесь тем, чтобы все они хорошо чувствовали себя при одинаковом ph воды. Но, тем не менее, многие аквариумисты всё равно пытаются держать рыб в той воде, которая им не подходит. Рыбы могут жить( и даже долго) в той воде, которая не соответствует их запросам по ph, но вот размножение в такой воде довольно затруднительно, если не сказать, невозможно. Но у некоторых рыб размножение в природе происходит по мере того, как в водоёме меняется ph. Поэтому для разведения их в условиях аквариума, нам приходится искусственно менять эти показатели. Есть несколько способов понизить pH: (1) Фильтрация с торфом. (2) Помещение коряги в аквариум (3) Введение углекислого газа CO2 (4) Использование кислотного буфера (5) Частичная подмена воды более мягкой водой или водой с обратным осмосом. Также есть несколько способов увеличить уровень pH: (1) мощная аэрация воды. Повышение содержания кислорода автоматически снизит содержание углекислого газа CO2. (2) Добавление в наполнитель фильтра известняка или коралловых частиц. (3) Использовать в аквариуме камни с высоким содержанием растворимого известняка или использовать коралловую крошку в качестве субстрата грунта. (4) Использовать алкалиновый (щелочной) буфер. Но запомните, что любые изменения в уровне Ph должны производиться плавно и постепенно!!! Скудно буферизованная вода (низкий kH или временная жёсткость) будет более подвержена резким колебаниям уровня pH, нежели хорошо буферизованная. Буфером может считаться грунт, имеющий в своем составе много известняка - для поддержания высокой жесткости воды. Также буфером может являться кусок дерева, коряга, которая подкисляет воду и понижает pH. Заметим, что буферизация и щелочность тесно связаны, т.к. фактически, щелочность является буфером, замедляющим изменение pH в воде. Как правило, жёсткая вода обычно имеет щелочной состав ( pH более 7 ) и является хорошим буфером. В то же время мягкая вода (pH ниже 7) – несколько кислее и в качестве буфера не годится. Постоянная жёсткость воздействует на уровень рН и для того, чтобы разобраться в том, как регулировать рН, мы должны понять, что же такое жесткость. Жёсткость воды. К тому времени, как попасть в нашу водопроводную систему и в наши краны, вода насыщается многочисленными растворёнными веществами. Жесткость – это измерение концентрации ионов металла, таких как кальций, магний, железо и цинк. Большинство из этих веществ попадают в водохранилища, подземные источники и водоёмы, когда дождь, омывая камни, захватывает с них эти элементы и уносит в землю. Большая честь пресной воды содержатся, в основном, соли кальция и магния плюс небольшое количество других элементов. Существует два вида жёсткости воды, на которые нужно обращать внимание (2) временная жесткость или щёлочность (её ещё часто называют карбонатной жёсткостью, измеряют в kH) Общая сумма постоянной и временной жесткости называется общая жёсткость. Изменяется в gH. Щёлочность или временная (карбонатная) жёсткость воды формируется при помощи карбонатных и бикарбонатных ионов (ионов кальция и магния). Временная жёсткость напрямую отражает способность воды к буферизации (то есть, способности воды поддерживать рН в стабильном состоянии). Временную жёсткость можно ликвидировать или уменьшить при помощи кипячения. Взгляните на внутренние стенки чайника или на головку душа – они покрыты карбонатной «коркой». Это то, что происходит с кальцием и магнием при воздействии высокой температуры – они отделяются от воды и становятся осадком или накипью. Вода же теряет свою временную жёсткость (поэтому она называется временной). Есть определённая связь между жёсткостью воды и буферизацией. Но при этом жесткость – это преимущественно продукт ионов кальция и магния, а буферизация обеспечивается ионами бикарбоната (гидрокарбонатом) и карбоната (ионами углекислой соли). Как я уже говорил, жёсткая вода обычно является прекрасным буфером, а мягкая вода таковым, как правило, не является. Впрочем, бывают исключения, когда в зависимости от составляющих микроэлементов в воде, жёсткая вода становится плохим буфером, а мягкая, напротив, хорошо буферизует. Для того чтобы определить качество и способность вашей местной водопроводной воды к буферизации, воспользуйтесь набором тестов для определения pH и временной карбонатной жесткости kH. Затем вычислите общую жесткость gH. Карбонатная или временная жёсткость показывает способность воды к буферизации или, как её ещё называют, способность воды абсорбировать и нейтрализовать лишние молекулы кислоты без изменения уровня pH. Вообразите, что буфер воды - это большая губка, и чем больше способность воды буферизовать кислоту, тем больше эта губка. Какая буферизация необходима для вашего аквариума? Чем выше карбонатная жёсткость воды kH (то есть, чем больше наша воображаемая губка-буфер), тем более устойчива вода к любым колебаниям уровня рН. Следовательно, уровень кН воды аквариума должен быть достаточно высоким, чтобы предотвратить скачки рН, которые случаются время от времени по независящим от нас причинам. Если в вашем аквариуме кН менее 4.5, то надо бы уделять побольше внимания уровню рН (то есть, периодически измерять его) до тех пор, пока не почувствуете уверенность в его устойчивости. Кстати сказать, буферизация – это, с одной стороны, очень хорошо, а с другой стороны не очень. Плюсом можно считать то, что во время азотного круга буфер заботится о постоянстве рН. Минус буферизации в том, что жесткая вода почти всегда является превосходным буфером, и, если вашим рыбам противопоказана повышенная жёсткость, то снижать её бывает довольно трудно при устоявшемся буфере.Буферизация зачастую ассоциируется с щёлочностью, но не следует путать такие понятия как щелочность воды и щелочная среда. Щелочность способствует лучшей буферизации, а щелочная среда – это среда, в которой щелочь несколько преобладает над кислотой. При щелочной среде уровень рН – чуть больше нейтрального, то есть, выше 7. Но не более 8. В то время как щёлочность – это состояние воды, где рН более 8 и созданы прекрасные условия для буферизации (стабилизации) рН… Аквариумы с низкой кН (карбонатной жёсткостью) требуют более частых продмен воды, чтобы контролировать уровень нитратов. Если этого не делать, в аквариуме будет постоянно «скакать» уровень рН. Как и рН, уровень kН возможно регулировать. То есть, уменьшать или повышать буферную способность воды. Способы повышения карбонатной жесткости: (1) Добавление в воду гидрокарбоната натрия (пищевая сода). Одна чайная ложка соды на 50 литров воды способна повысить уровень кН приблизительно на 4 OdH (oxidative dehydrogenation - окислительное дегидрирование) без какого-либо значительного влияния на сам уровень рН. (2) Использование в интерьере аквариума воздушного камня. Это пористый камень, который при помощи воздушной помпы и полой соединительной трубочки создаёт каскад пузырьков воздуха. Они, в свою очередь, будоражат поверхность воды, усиливая газообмен и уменьшают концентрацию углекислого газа СО2 в воде. (3) Использование имеющихся в продаже средств для искусственного повышения буферности воды. Способы снизить карбонатную жёсткость: (1) Впрыскивание углекислого газа СО2 в воду. (2) Применение обратного осмоса воды. Можно смешивать воду из водопровода и воду с обратным осмосом для достижения более низкой карбонатной жёсткости. (3) Использование имеющихся в продаже средств для искусственного снижения буферной способности воды. У рыб, живущих в неподходящих условиях, ослабляется иммунитет. Это приводит к тому, что рыбка часто болеет и не хочет размножаться. Дистиллированная вода – это не лучший выбор для аквариума. У неё по определению нет рН вообще. Это значит, что при попадании в аквариум кислоты (какой угодно), уровень рН очень резко подскочит, и это станет серьёзным стрессом для рыбы. Из-за своей нестабильности дистиллированная вода (и вообще любая чистая от минеральных примесей вода) практически не используется в аквариумистике. А если используется, то в неё искусственно добавляют соли кальция и магния, чтобы повысить gH и рН. Несколько слов о том, что такое gH Общая жесткость (англ: General hardness), измеряется в gH и сообщает нам о концентрации преимущественно ионов магния и кальция в жидкости. Ионы других минералов тоже могут влиять на общую жесткость воды, но их влияние столь незначительно и трудно определимо, что почти никогда они в расчет не берутся. Имейте ввиду, что когда о рыбе говорят «она предпочитает жёсткую (мягкую) воду», то речь идёт именно об общей жёсткости (gH). Не нужно путать с карбонатной временной жёсткостью kH. Нужно сказать, что gH не влияет на уровень рН воды, хотя «жёсткая» вода, как правило, более щелочная в силу того, что общая жёсткость связана с карбонатной жёсткостью kH. Неподходящая жёсткость (gH) воды негативно влияет на усвоение питательных веществ через мембрану клеток и выведение продуктов распада, может повлиять на оплодотворение икры, функционирование внутренних органов рыбы, таких как почки и на рост животных. Вообще-то, большинство рыб и растений способны благополучно приспосабливаться к изменяющимся условиям, в том числе и к непривычной жёсткости (или, наоборот, мягкости) воды. Но размножение рыбы в условиях неподходящей жёсткости весьма затруднительно, а иногда и совершенно невозможно. » Спасибо сказали: «
|
| big-alex |
 26.3.2009, 10:07 26.3.2009, 10:07
Сообщение
#19
|
 Поддерживает разговор  Группа: Пользователи Сообщений: 107 Регистрация: 16.3.2009 Из: Новосибирск Пользователь №: 90 850 Репутация:  15 15  |
Каким должен быть уровень нитратов В аквариуме не должно быть нулевого уровня нитратов. В подобном случае они могут оказаться лимитирующим фактором роста растений и поглощение мим фосфатов прекратится. Такая ситуация может встретится в сильно заросшем аквариуме (особенно быстрорастущими растениями), при недостаточном количестве рыб. безусловно, нулевой уровень нитратов не означает, что растения их не получают. Он лишь указывает на то, что растения поглощают нитраты (и аммиак/аммоний/нитриты, не дожидаясь их преобразования в нитраты в результате био-фильтрации) с такой же скоростью или быстрее, чем они вырабатываются в системе. Как показывает практика, небольшой уровень нитратов (около 2-5 mg/l) желателен в аквариуме. чтобы была уверенность. что фосфаты являются лимитирующим фактором в росте растений (и водорослей). Обычно, при нулевом уровне нитратов через несколько дней начинается рост уровня фосфатов в воде. При добавлении нитратов - он опять падает до нуля. Если фосфаты на нулевом уровне в аквариуме, то наличие нитратов не вызовет роста водорослей. Следует проверять уровень нитратов, если есть подозрение. что их не хватает. Признаком нехватки нитратов является пожелтение и отмирание старых листьев - они как-бы растворяются в воде (за счет миграции азотных соединений к молодым листьям). В подобном случае следует добавить нитратов - лучше всего KNO3. Немного добавлю, нитраты и фосфаты не являются стимуляторами роста водорослей это уже доказано и подтверждено на практике, нормальным можно считать уровень нитратов 10 фосфатов 1 мг/л можно и больше главное сохранять пропорцию, я вношу нитраты и фосфаты периодически в пропорции 15/1, никаких водорослевых вспышек нет, при приближении нитратов к 50 мг/л начали чесаться рыбы и умерло несколько расбор, добавки прекратил, сейчас сыплю аммиачную селитру, 1 горошина на 100 литров, растения азот предпочитают в амонийной форме. » Спасибо сказали: «
|
| spec11 |
 23.8.2009, 19:34 23.8.2009, 19:34
Сообщение
#20
|
 МЕГА флудер     Группа: Sibnet-club Сообщений: 8 291 Регистрация: 10.12.2008 Из: 53°21′24″ с. ш., 83°47′14″ в. д. Пользователь №: 66 131 Репутация:  1456 1456  |
Проблема подменной воды. Хлор. Аммиак
 Как правильно подготовить водопроводную воду для аквариума? Почему у рыб ухудшается состояние после залива свежей воды? Нужно ли применять кондиционеры воды? Эти и другие вопросы рассмотрены в статье. » Спойлер (нажмите, чтобы прочесть) « Хлор - в свободном состоянии при нормальных условиях двухатомный газ желто-зеленого цвета, относится к галогенам. Хорошо растворим в воде. Впервые хлор был получен в 1774 г. в Швеции Шееле взаимодействием соляной кислоты с пиролюзитом. Однако только в 1810 г. Дэви установил, что хлор - химический элемент и назвал его Chlorine (от греческого "Chloros" - желто-зеленый). В водопроводную воду хлор вносится с целью ее обеззараживания. В настоящее время обычно используется гипохлорит натрия (NaClO), который затем разлагается распаданием на хлор, кислород и соли. В больших концентрациях хлор ядовит. Определить высокую концентрацию хлора можно по характерному запаху этого газа, знакомому многим людям, посещавшим плавательные бассейны, но надежнее всего воспользоваться специальным тестом. Кстати, в водопроводной воде хлор содержится не всегда, ибо в некоторых случаях в системе водоканала для обеззараживания воды применяется озонирование. Для большинства аквариумных рыб предельная концентрация хлора в воде - 0,25 мг/л, а концентрация 1 мг/л является летальной. При более низких концентрациях, он тоже вредит рыбе, повреждая жабры. Основными методами очистки подменной воды от хлора - отстаивание воды и химическая очистка. Отстаивание воды. Хлор относительно непостоянен в воде, самостоятельно улетучиваясь в атмосферу. Касательно длительности отстаивания водопроводной воды перед заливом в аквариум в литературе обычно называется цифра 1-2 суток. Хотя авторы книги "Современный аквариум и химия" рекомендуют более длительный срок: 5-6 дней. Резервуар для отстаивания воды должен иметь достаточно большую поверхность взаимодействия с воздушной средой. Процесс удаления хлора из воды можно ускорить, если при заливе воды в ведро для отстаивания пустить из водопроводного крана сильную струю, либо лить воду из душа, а также если в ходе отстаивания воду аэрировать. Следует добавить, что при отстаивании водопроводная вода освобождается от ряда других вредных примесей, не рассмотренных в этой статье. Химическая очистка. Самым быстрым способом удаления хлора из воды является применение химического препарата-дехлоратора, который вступая в химическую реакцию с растворенным в воде хлором, превращая его в малотоксичные вещества. Обычно для этого используется тиосульфат натрия Na2S2O3, восстанавливающий хлор до хлорид-ионов: 4Cl2 + Na2S2O3 + 5H2O = Na2SO4 + H2SO4 + 8HCl . Тиосульфат натрия содержится в популярных у аквариумистов препаратах по подготовке воды (AquaSafe, Aquatan, Тар Water, Stress Coat и др.). Но при их использовании следует иметь в виду, что указанные в инструкции дозировки являются усредненными, в то время как содержание хлора в водопроводной воде может колебаться в зависимости от местности, времени года и других условий. В моей практике имеется случай когда в после обработки аквариума кондиционером Tetra AquaSafe вся запущенная в аквариум стартовая рыба данио рерио быстро погибла с явными признаками сильного отравления хлором, т.е. рекомендованная производителем дозировка очевидно оказалась недостаточной. Более надежным способом является адсорбционный метод - прогон хлорированной водопроводной воды через активированный уголь, хлор адсорбируется на нем, и вода освобождается от токсичного компонента. На практике этот способ очистки реализуется посредством проточного угольного фильтра, через который пропускается вода из-под крана, либо оснащения емкости для водоподготовки внутренним фильтром с углем. Кстати, необязательно покупать в зоомагазине специальный аквариумный уголь, бытовой активированный уголь работает не хуже. Вообще, вопреки сложившемуся стереотипу, не стоит отклонять возможность использования для аквариумного хозяйства бытовых фильтров водоподготовки. Единственное, нужно четко соотносить стоящие задачи и состав используемых фильтрующих элементов. В числе способов по очистке воды от хлора называется также кипячение, либо нагревание до температуры 80-90°C. Кипячение делает воду "мертвой" с точки зрения содержания полезных микроэлементов и резко снижает карбонадную жесткость. Кроме того, нагревание воды до температуры кипения или близкой к ней не может быть произведено в штатных емкостях для водоподготовки. Для этого требуются специальные металлические емкости и длительное время для охлаждения воды до нормальной температуры. Многие аквариумисты льют в аквариум хлорированную воду прямо из-под крана. Мне даже приходилось слышать мнение, что хлор в разумных дозах положительно сказывается на функционировании аквариумной биосистемы - замедляет рост водорослей, дезинфицирует воду, укрепляет у рыб иммунитет к воздействию ядовитых веществ. Действительно, так можно делать, поскольку при заливке в налаженный аквариум хлор в течение нескольких секунд нейтрализуется во взаимодействии с местной средой и не успевает навредить. Хотя, например, для некоторых видов танганьикских цихлид при массированной подмене воды и этих нескольких секунд оказывается достаточно, чтобы убить их. В данной ситуации губительно даже не столько само отравление хлором, сколько стресс от резкой перемены параметров воды в аквариуме. Поэтому количество единоразово подмениваемой воды должно увязываться со степенью прихотливости того или иного вида рыб, а если рыба ранее содержалась в аквариуме, куда заливалась очищенная от хлора вода, следует приучать ее к хлору постепенно, поэтапно увеличивая объем подмен. Но лучше все-таки заливать воду, предварительно очистив ее, тем более, что как показано выше, сделать это несложно. Особенно опасно использовать хлорированную воду в период весеннего паводка, когда для лучшего обеззараживания воды концентрацию хлора в ней повышают. Еще одним химическим веществом, применяемым предприятиями водоснабжения для обеззараживания воды является хлорамин, смесь хлора с аммиаком. Как считается, хлорамин "имеет значительные преимущества, т.к. его бактерицидное действие сохраняется в течение большего времени, чем у хлора, и, кроме этого, хлорамины не придают воде неприятного запаха и привкуса, как хлор и его соединения с веществами, содержащимися в воде". С точки зрения же аквариумистики все абсолютно наоборот. Хлорамин - это огромное зло и головная боль. Тиосульфат натрия способен нейтрализовать только часть хлорамина - хлор, тогда как аммиак при этом остается в воде, хотя существует предположение, что хлорамин все-таки диссоциирует в воде не полностью и образует комплексы, которые поддаются адсорбированию углем. К счастью, в нашей стране практика хлораминирования водопроводной воды не получила широкого распространения. Однако следует иметь в виду, что хлорамин может образоваться и самостоятельно в результате взаимодействия хлора водопроводной воды и аммиака. Аммиак - бесцветный газ с удушливым резким запахом, хорошо растворяется в воде, спирте и ряде других органических растворителей. Вода содержащая летальные дозы аммиака не имеет запаха. В воде существует в виде свободного аммиака (NH3) и ионов аммония (NH4+), а также солей аммония. В аэробных условиях окисляется до нитритов и нитратов. Впервые аммиак был получен в чистом виде в 1774 г. английским химиком Дж. Пристли. Он нагревал нашатырь (хлорид аммония) с гашеной известью (гидроксид кальция). В 1784 г. К. Бертолле установил элементный состав этого газа, который в 1787 г. получил официальное название "аммониак". Это название сохраняется и ныне в большинстве западно-европейских языков (нем. ammoniak, англ. ammonia, фр. ammoniaque), сокращенное название "аммиак", которым мы пользуемся, ввел в обиход русский химик Я.Д. Захаров в 1801 г. Неионизированный аммиак является сильно токсичным соединением: летальный уровень составляет примерно 0,2-0,5 мг/л для различных видов рыб. Негативное воздействие в более малых дозах приводит также к резкому снижению иммунитета рыбы, что нередко прочти сразу же проявляется в виде "горения" плавников и помутнения тканей. Ионы аммония тоже токсичны, но в меньшей степени. Соотношение концентраций NH3 и NH4+ в воде также зависит от ее кислотности и температуры: в кислой и холодной воде аммиак практически отсутствует, в щелочной и теплой среде его концентрация возрастает. Аммиак хорошо известен аквариумистам как первый этап так называемого "азотного цикла". Отработаны и методы борьбы с ним в аквариуме. В современных аквариумах данная проблема эффективно решается с помощью биофильтрации и, как правило, не вызывает у аквариумиста больших затруднений. Но есть и другой аспект, а именно содержание аммиака уже в водопроводной воде. Открытие этого неприятного факта нередко вызывает удивление и даже шок. Между тем ничего "удивительного" здесь нет, ибо официально установленная предельно допустимая концентрация (ПДК) содержания аммиака и ионов аммония в водоемах хозяйственно-питьевого и культурно-бытового водопользования составляет: 2 мг/л по азоту или 2,6 мг/л в виде иона аммония, и показатели тестов водопроводной воды на аммиак 0,3-0,5 мг/л и более являются совершенно "нормальным" явлением. В Санкт-Петербурге, например, по осени этот показатель регулярно достигает единицы. Тоже самое имело место и в Москве слякотной зимой 2006/07 гг., когда резкие ухудшения самочувствия рыб после подмен воды заставили меня впервые всерьез озадачиться изучением данной проблемы. Кстати, для сравнения: ПДК аммоний-иона для рыбохозяйственного производства - 0,5 мг/л, для вод озера Байкал - 0,04 мг/л; для питьевой воды в странах Евросоюза - 0,5 мг/л. Откуда берется аммиак в водоемах и водопроводной воде? В отличие от хлора, аммонийные соединения попадают в водопроводную воду сами собой, без непосредственного участия человека, а вернее сказать при косвенном его участии. Растворенный аммиак (аммоний-ион) поступает в водные объекты с поверхностным и подземным стоком, атмосферными осадками, а также со сточными водами промышленных предприятий. В водоемах аммиак также образуется при разложении азотсодержащих органических веществ (в частности аммонийные соединения в больших количествах входят в состав удобрений). Основными источниками загрязнения являются животноводческие фермы, хозяйственно-бытовые сточные воды, поверхностный сток с сельхозугодий, а также сточные воды предприятий пищевой и химической промышленности. Здесь же следует отметить, наличие сезонных колебаний концентрации аммиака в водоемах: в период весеннего паводка и осенних дождей она существенно возрастает. В. Ковалев в статье "Кислотный дождь" говорит еще об одной причине. Из-за сильного загрязнения промышленными выбросами в выпадающих на землю осадках содержится диоксид серы и серная кислота. В процессе таяния снега происходит преимущественная потеря растворенных ионов, поскольку они стремятся накапливаться снаружи зерен льда, из которых состоят сугробы. Это означает, что на ранних стадиях таяния выносится именно растворенная серная кислота. Возможно двадцатикратное повышение ее концентрации в талой воде. В это время,- указывает В. Ковалев,- вода в водопроводе может стать гораздо кислее обычного, а также содержать повышенное количество аммония и сернокислого алюминия. С помощью сернокислого алюминия воду на водопроводных станциях "коагулируют" - алюминий дает коллоидный осадок, он отфильтровывается сам и заодно извлекает из воды множество других загрязнителей. Кислая вода очень плохо коагулируется. Поэтому ее специально подщелачивают. Как правило, это делают с помощью гидроксида аммония (NH4OH) или аммиака. Таким образом он оказывается затем в водопроводной воде обычно в виде ионов аммония или хлораминов. Несколько слов о тестах. Во-первых, в зоомагазинах продаже имеется большое предложение тестов различных производителей. Новички часто задают вопрос, какие тесты нужны и какого производителя предпочесть. Для контроля процесса нитрификации в аквариуме и работы биофильтра приобретать тест на аммиак едва ли имеет смысл - более целесообразно контролировать содержание нитрита (хотя и он после запуска аквариума скорее всего будет пылиться на полке). Однако если из-под крана течет вода с высоким содержанием аммиака, то иметь такой тест необходимо. В отношении производителей из того, что я пробовал, самые точные - тесты Tetra, а самые практичные - Aquarium Pharmaceuticals. Не рекомендую использовать тесты Sera и НИЛПА. Во-вторых, тест позволяет определять лишь общую концентрацию аммонийных соединений, не отделяя аммиак от ионов аммония, хлорамина, аммонийных солей и других соединений, токсичность которых неравнозначна. Теоретически существуют специальные таблицы для определения процентного соотношения концентраций NH3 и NH4+ в зависимости от показателей pH и температуры воды. Но на практике это не вполне применимо, а главное не проверяемо. Поэтому, в отличие, например, от нитрита, четко оценить степень угрозы мы не имеем возможности. Методы удаления аммиака из воды. Биологическая очистка. Применительно к водоподготовке использование процесса нитрификации может быть реализовано посредством временного переноса погружного фильтра со сформировавшейся колонией нитрифицирующих бактерий в наполнителе из аквариума в емкость для подготовки воды. При этом вода должна быть предварительно отстояна или химически очищена от хлора, а после выполнения своей работы фильтр должен быть возвращен обратно в аквариум. Все это не слишком удобно. Кроме того, если используется один водоотстойник на несколько аквариумов, возникает опасность распространения возбудителей заболеваний из того аквариума, откуда взят фильтр. Фитофильтр. В последнее время много говорят об этом, в основном применительно к нитратам, но в принципе, растения могут поглощать и аммиак. На практике мне еще ни разу не доводилось увидеть фитофильтр в действии. Кипячение воды. После недолгого кипячения в 5-10 минут тест не обнаруживает присутстия аммиака. Данный метод является одним из самых простых и эффективных, но, к сожалению, как уже ранее отмечалось, малопригоден для аквариумистики. Нагревание. При повышении температуры растворимость NH3 падает и он испаряется. Данный метод по-видимому позволяет снизить концентрацию свободного, т.е. наиболее токсичного, аммиака, хотя общая концентрация аммонийных соединений визуально по тесту изменяется не слишком обнадеживающе. При всех очевидных достоинствах недостатком данного метода является опять-таки невозможность нагревания в штатных емкостях до высоких температур, время, требующееся для охлаждения, и невозможность проконтролировать результат с помощью теста. Обратный осмос. Процесс обессоливания воды, в котором из воды на 99% удаляются минеральные соли, органические вещества и микроорганизмы. Принцип работы установки обратного осмоса основан на продавливании воды через полупроницаемые осмотические мембраны. В результате чего одна часть воды практически полностью обессоливается и идет на использование, другая же часть, содержащая соли, частью сбрасывается в канализацию, а частью повторно подается на мембраны. По своим характеристикам осмосная вода близка к дистилляту. Для использования в аквариуме ее требуется обогатить солями. Для этого, в частности, могут быть использованы соли Sera mineral salt. Обратный осмос применяется в аквариумистике, но по понятным обстоятельствам пригоден далеко не для каждого и не для любых условий. Аэрация. Принцип аэрации для удаления применяется в бытовых фильтрах для дегазации растворенных газов - сероводород, аммиак, метан и т.д. Известно, также что в индустриальных рыбоводных хозяйствах и инкубационных цехах производят водоподготовку, используя дегазаторы-аэраторы. Дегазация достигается барботированием воздуха в тонкий слой текущей воды. Соотношение воздуха и воды (5-10):1. При таком барботаже вода бурлит под воздействием большого количества проходящих через нее пузырьков воздуха. При этом из нее быстро (в течение нескольких секунд) удаляется аммиак, метан, сероводород и другие нежелательные для рыб газы, если они были в воде. В условиях домашнего аквариумного хозяйства аэрация дает хорошие результаты в сочетании с нагреванием. Так, по опыту израильского аквариумиста Якова Оксмана, нагрев водопроводной воды до приблизительно до 50°C с одновременной мощной продувкой воздухом и созданием бурления воды с помощью компрессора уменьшает концентрацию аммиака/аммония до трети. Однако напомним здесь же, что сильное насыщение воды кислородом ведет к повышению pH, что нежелательно как с точки зрения требования согласованности параметров аквариумной и подменной воды, так и увеличения процентного содержания неионизированного аммиака в воде с высоким показателем pH. Воздействие кислотой - при этом аммиак и ионы аммония преобразуются в малотоксичные соли аммония. Данный метод, используется в химии, но для аквариумистики едва ли приемлем. Ионообмен. В фильтре-поглотителе нитрогенов используются сильноосновные анионообменные смолы. Они удаляют из воды азотнокислые анионы, замещая их ионами хлоридов. В качестве регенеранта используется раствор соли NaCl. Данный способ реализован в бытовых фильтрах по очистке питьевой воды. Недостаток бытовых фильтров для квартиры заключается в их слабой производительности, затрудняющей приготовление достаточного количества подменной воды для аквариума. В сельской местности применяются более крупногабаритные и производительные водоочистные установки для коттеджей. Эти фильтры позволяют также освобождать воду от нитратов, содержание которых в некоторых районах превышает все мыслимые для аквариумистики и употребления воды в пищу нормы. Следует иметь в виду, что фильтрации через ионообменные смолы приводит к деминерализации и снижению жесткости воды. Фильтрация через цеолит. Термин цеолит (в переводе с греческого "кипящий камень") включает целое семейство минералов - водосодержащих алюмосиликатов с катионами калия, натрия, кальция и магния. В 1756 г. Ф. Кронштедт обнаружил вспучивание (увеличение объема образца, сопровождающееся выделением воды) стильбита (минерала семейства гидратированных силикатов алюминия) при нагревании. Он и ввел термин "цеолит". Существуют природные и искусственно синтезированные цеолиты (пермутиты), которые находят широкое применение в водоочистительных приборах как адсорбенты, ионообменники и молекулярные сита. Подвижность катионов и их способность к ионному обмену определяет высокие сорбционные свойства цеолитов на уровне ионообменных смол. В упрощенном виде это можно описать так: цеолит "забирает" аммиак и "обменивает его на соль". Однако, как показала практика, наши представления о способности цеолита очищать воду от аммиака несколько преувеличены. В реальности не все виды цеолитов пригодны для этого. Например, цеолит фирмы AquaEl, будучи загруженным мною в фильтр, судя по показаниям тестов, никак не влиял на концентрацию аммиака, либо для выполнения этой задачи он требуются в объеме, гораздо большем, чем способен вместить в себя аквариумный фильтр. Не слишком обнадеживающими оказались и испытания в проточном фильтре цеолитов ряда других производителей. Можно предположить, что для эффективной очистки нужен не разовый, а многократный прогон через фильтр, поэтому применение цеолита в проточных фильтрах не дает столь сильного эффекта, как использование активированного угля для удаления хлора. Специальные кондиционеры, позволяющие обезвреживать аммиак и хлорамиды, временно связывая в безопасные химические соединения. Причем тесты на аммиак после их применения будут давать по-прежнему положительные результаты, но аммиак будет уже в нетоксичной форме. К числу таких препаратов относятся Ammo-lock производства Aquarium Pharmaceuticals и Sera Toxivec. Их действие более подробно будет рассмотрено в отдельной публикации. Здесь же ограничимся рекомендацией не увлекаться этими средствами и использовать их только в экстренных случаях. Для регулярного использования в водоочистке вышеназванные кондиционеры не пригодны. Открытым остается вопрос, может ли аммиак адсорбироваться активированным углем. Мои эксперименты и опыт ряда коллег дали отрицательный ответ, однако на форуме израильских аквариумистов было изложено противоположное мнение, также подкрепленное вполне конкретным практическим опытом и высказано предположение, что возможно, в первом случае мы имеем дело "с какой-то иной химической связкой аммония, не летучей и не сорбирующейся". Итак, если подытожить, приходится признать, что с аммиаком дело обстоит не столь легко, как с удалением хлора. Поэтому рекомендуется обратить внимание и на то, чтобы правильно проводить подмену воды. Напомню, в данном случае опасно не столько само отравление, сколько стресс от резкой перемены параметров водной среды. Как показывает опыт, рыба обычно достаточно неплохо переносит кратковременное повышение концентрации аммонийных соединений до 1 мг/л и даже до 2 мг/л, но только при условии, что эта концентрация наращивалась постепенно, например, при запуске аквариума. Иначе происходит при быстром заливе в аквариум воды с аналогичной аммониевой концентрацией. Да, не стоит беспокоиться о том, что попавший в аквариум аммиак останется там надолго, он будет очень быстро переработан и устранен биофильтрацией, но резкое изменение (увеличение) его концентрации может нанести существенный ущерб здоровью рыб, а применительно к некоторым особо чувствительным видам даже вызвать их гибель, в особенности, если высок уровень содержания нитратов в аквариуме. Что можно сделать для минимизации негативного воздействия? Во-первых, не менять слишком много воды за раз. Во-вторых, не торопиться и заливать воду из шланга тонкой струей. В-третьих, воду для снижения негативного воздействия аммиака на рыб можно подсаливать (5 столовых ложек на 100 л). В-четвертых, применять кондиционеры-антистрессы, такие как Tetra AquaSafe. Вопреки распространенному мнению, подкрепленному рекламными заявлениями производителей, эти препараты не обладают большими возможностями по очистке воды от вредных примесей (за исключением разве что входящего в их состав тиосульфата натрия, не способного однако защитить от аммиака), но зато содержат особые защитные коллоиды, предохраняющие слизистую оболочку и кишечную полость рыб и уменьшающие таким образом шок от воздействия ядовитого вещества. И я имел возможность сравнить и убедиться, что эти кондиционеры реально работают. На вопрос какой из них лучше всех, я бы назвал Aquavital Conditioner фирмы Aquarium Munster, а явным аутсайдером - Aquatan фирмы Sera. Здесь же можно дать ответ на вопросы, которыми наверняка на определенном этапе озадачивался каждый аквариумист. Обрабатывать ли кондиционером подменную воду или вносить его непосредственно в аквариум? Если первое, то лить ли кондиционер загодя или в ходе подмены воды? И исходя из какого объема рассчитывать дозировку: объема аквариума или емкости для отстаивания? Я считаю правильным вносить кондиционер во время подмены, так чтобы содержащиеся в нем коллоиды имели максимальную эффективность. Рассчитывать дозу нужно исходя из объема аквариума. Часть кондиционера можно добавить в емкость для отстаивания минут за десять до перекачки воды в аквариум, чтобы дехлоратор мог сделать свою работу, а остальную часть - непосредственно в аквариум. Наряду с хлором и аммиаком водопроводная вода может содержать нитраты, а также избыток двухвалентного железа... Для обезжелезивания воды используется отстаивание, а в качестве радикальной меры - регенерируемый фильтр, работающий методом каталитического окисления двухвалентного железа с последующим осаждением гидроокиси железа в фильтрующей загрузке, либо обратный осмос. Для устранения нитратов - ионообменный фильтр, либо обратный осмос. Здесь же следует сказать пару слов о температуре воды. В зимнее время из холодного течет ледяная вода, поэтому для достижения приемлемой температуры приходится перемешивать ее с водой из горячего крана. Последняя гораздо хуже по качеству (это ощутимо даже по вкусу), поскольку горячие трубы из-за более агрессивной среды находятся обычно в худшем состоянии. Избежать этого можно с помощью проточного водонагревателя, а при использовании емкости для отстаивания поместить в нее аквариумный водонагреватель или дождаться пока вода естественным образом достигнет комнатной температуры. Е. Грановский, 2009 г. » Спасибо сказали: «
|
  |
1 чел. просматривают этот форум (гостей: 1, скрытых пользователей: 0)
Пользователей: 0
| Текстовая версия | Сейчас: 20.4.2024, 11:32 |